|
ΒΡΑΒΕΙΟ ΝΟΜΠΕΛ ΧΗΜΕΙΑΣ 2013
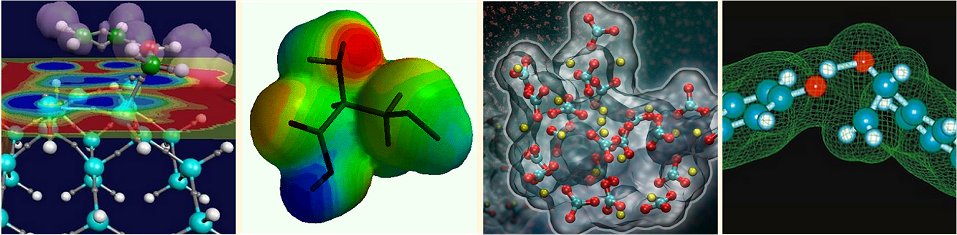
"Οι χημικοί χρησιμοποιούσαν μοντέλα για να αναπαραστήσουν τα χημικά μόρια με τη χρήση πλαστικών σφαιρών για τα χημικά άτομα και ραβδίων για τους χημικούς δεσμούς. Σήμερα όμως χρησιμοποιούν τους ηλεκτρονικούς υπολογιστές για να δημιουργήσουν μοντέλα και να μελετήσουν τις χημικές αντιδράσεις. Στη δεκαετία του 1970 οι επιστήμονες Martin Karplus, Michael Levitt και Arieh Warshel έβαλαν τις βάσεις για τη δημιουργία εξειδικευμένων προγραμμάτων τα οποία χρησιμοποιούνται για την κατανόηση και την πρόβλεψη χημικών διεργασιών. Τα μοντέλα των ηλεκτρονικών υπολογιστών που καθρεφτίζουν τη φυσική πραγματικότητα έχουν γίνει εξαιρετικά χρήσιμα για την πρόοδο της επιστήμης. Σημαντικός αριθμός νέων ανακαλύψεων και τεκμηρίωσης χημικών διεργασιών στη Χημεία του σήμερα έχουν επιτευχθεί με την Υπολογιστική Χημεία. Οι χημικές αντιδράσεις σε πολλές περιπτώσεις γίνονται με ταχύτητα φωτός. Μέσα σε κλάσματα χιλιοστού του δευτερολέπτου, τα ηλεκτρόνια μετακινούνται από το ένα άτομο στο άλλο. Η Κλασική Χημεία είχε μεγάλη δυσκολία να μελετήσει τις ταχύτατες χημικές αντιδράσεις, ήταν σχεδόν αδύνατο να πειραματισθεί για το κάθε μικρό βήμα μεταβολών των χημικών διεργασιών. Η βοήθεια που προσέφεραν οι βραβευμένοι με το Βραβείο Νόμπελ Χημείας επιστήμονες με τις μεθόδους των μοντέλων τους ήταν σημαντική. Οι επιστήμονες χρησιμοποίησαν τους ηλεκτρονικούς υπολογιστές για να αποκαλύψουν διάφορες χημικές διεργασίες όπως, για παράδειγμα, ο καταλυτικός καθαρισμός των καυσαερίων αυτοκινήτων ή την πορεία της φωτοσύνθεσης των πράσινων φύλλων των φυτών. Οι επιστημονικές εργασίες των Karplus, Levitt και Warshel είχαν επαναστατική αξία για την επιστήμη της χημείας γιατί κατάφεραν να τοποθετήσουν την Κλασική Φυσική του Νεύτωνα δίπλα στις εντελώς διαφορετικες αρχές της Κβαντικής Φυσικής. Προηγουμένως, οι χημικοί είχαν να διαλέξουν τη μία ή την άλλη θεωρία. Η ισχύς της Κλασικής Φυσικής ήταν ότι οι υπολογισμοί ήταν απλοί και μπορούσαν να χρησιμοποιηθούν για μοντέλα μεγάλων χημικών μορίων (μεγάλο μοριακό βάρος). Η κύρια αδυναμία της ήταν ότι δεν μπορούσε να προσομοιώσει χημικές αντιδράσεις. Για τον σκοπό αυτό οι χημικοί έπρεπε να χρησιμοποιήσουν την κβαντική φυσική. Αλλά τέτοιοι υπολογισμοί απαιτούσαν υπολογιστές με εξαιρετικά μεγάλη υπολογιστική ισχύ και γι αυτό εφαρμόζονταν μόνο σε μικρού μοριακού βάρους χημικά μόρια. Οι βραβευμένοι με το Νόμπελ Χημείας του 2013 πήραν τις καλύτερες μεθόδους και από τα δύο είδη θεωριών και ανακάλυψαν μεθόδους που κάνουν χρήση τόσος της Κλασικής, όσο και της Κβαντική Φυσικής. Για παράδειγμα, στην προσομοίωση για το πώς τα φάρμακα υπόκεινται σε σύζευξη με την πρωτεΐνη-στόχο στον βιολογικό οργανισμό, ο υπολογιστής εκτελεί κβαντικούς θεωρητικούς υπολογισμούς για τα χημικά άτομα που βρίσκονται στην πρωτεΐνη στόχο και αλληλεπιδρούν με το φάρμακο. Για το υπόλοιπο μόριο της μεγάλου μοριακού βάρους πρωτεΐνης η προσομοίωση χρησιμοποιεί υπολογισμούς της Κλασικής Φυσικής. Οι ηλεκτρονικοί υπολογιστές σήμερα είναι εργαλείο μεγάλης αξίας για τους χημικούς όπως και ο δοκιμαστικός σωλήνας για χημικές αντιδράσεις στο παρελθόν. Οι προσομοιώσεις είναι τόσο ρεαλιστικές που μπορούν να προβλέψουν την πορεία και το αποτέλεσμα των κλασικών χημικών αντιδράσεων. Οι τρεις βραβευμένοι επιστήμονες εργάσθηκαν για πολλά χρόνια με ηλεκτρονικές προσομοιώσεις οι οποίες συνδύασαν κβαντικούς μηχανισμούς, ερμηνεύοντας τη διάσπαση και τον σχηματισμό χημικών δεσμών, με κλασικούς Νευτώνιους μηχανισμούς, που μπορούν να μελετήσουν τη μετακίνηση των πρωτεϊνικών μορίων. Το τελικό αποτέλεσμα των εργασιών αυτών, πιθανολογείται ότι θα είναι η ικανότητα να υπολογισθούν με ηλεκτρονικούς υπολογιστές πολύπλοκες χημικές διεργασίες και να γίνει ικανή η προσομοίωση ενός ολόκληρου ζωντανού οργανισμού σε μοριακό επίπεδo, κάτι που αποτελεί όνειρο για τον καθηγητή Levitt".
Επιστημονικές Δημοσιεύσεις - "All-Atom Empirical Potential for Molecular Modeling and Dynamics Studies of Proteins", A. D. MacKerell, Jr., D. Bashford, M., R. L. Dunbrack, Jr., J. D. Evanseck, M. J. Field, S. Fischer, J. Gao, H. Guo, S. Ha, D. Joseph-McCarthy, L. Kuchnir, K. Kuczera, F. T. K. Lau, C. Mattos, S. Michnick, T. Ngo, D. T. Nguyen, B. Prodhom, W. E. Reiher, III, B. Roux, M. Schlenkrich, J. C. Smith, R. Stote, J. Straub, M. Watanabe, J. Wiórkiewicz-Kuczera, D. Yin, and M. Karplus , J. Phys. Chem. B, 1998, DOI: 10.1021/jp973084f - "Solvation. A molecular dynamics study of a dipeptide in water", Peter J. Rossky and Martin Karplus , J. Am. Chem. Soc., 1979. DOI: 10.1021/ja00502a001 - "A Comprehensive Analytical Treatment of Continuum Electrostatics", Michael Schaefer and Martin Karplus , J. Phys. Chem., 1996. DOI: 10.1021/jp9521621 - "A QM/MM Implementation of the Self-Consistent Charge Density Functional Tight Binding (SCC-DFTB) Method", Qiang Cui, Marcus Elstner, Efthimios Kaxiras, Thomas Frauenheim, and Martin Karplus, J. Phys. Chem. B, 2001. DOI: 10.1021/jp0029109
- "Free
Energy Simulations Come of Age: Protein−Ligand Recognition", Thomas
Simonson, Georgios Archontis, and Martin Karplus ,
Acc. Chem. Res., 2002. DOI: 10.1021/ar010030m - "Calibration and Testing of a Water Model for Simulation of the Molecular Dynamics of Proteins and Nucleic Acids in Solution", Michael Levitt, Miriam Hirshberg, Ruth Sharon, Keith E. Laidig, and Valerie Daggett, J. Phys. Chem. B, 1997. DOI: 10.1021/jp964020s - "Extreme conformational flexibility of the furanose ring in DNA and RNA", Michael Levitt and Arieh Warshel, J. Am. Chem. Soc., 1978. DOI: 10.1021/ja00477a004 - "Induced peptide conformations in different antibody complexes: molecular modeling of the three-dimensional structure of peptide-antibody complexes using NMR-derived distance restraints", Tali Scherf, Reuben Hiller, Fred Naider, Michael Levitt, and Jacob Anglister, Biochemistry, 1992. DOI: 10.1021/bi00145a004 - "Probing antibody diversity by 2D NMR: comparison of amino acid sequences, predicted structures, and observed antibody-antigen interactions in complexes of two antipeptide antibodies", Rina Levy, Olga Assulin, Tali Scherf, Michael Levitt, and Jacob Anglister, Biochemistry, 1989. DOI: 10.1021/bi00444a006 - "NMR-derived model for a peptide-antibody complex", Barbara Zilber, Tali Scherf, Michael Levitt, and Jacob Anglister, Biochemistry, 1990. DOI: 10.1021/bi00495a004
- "Detailed
Hydration Maps of Benzene and Cyclohexane Reveal Distinct Water Structures", Tanya
M. Raschke and Michael Levitt, J. Phys. Chem. B, 2004.
DOI: 10.1021/jp049481p - "Calculation of ground and excited state potential surfaces of conjugated molecules. I. Formulation and parametrization", A. Warshel and M. Karplus , J. Am. Chem. Soc., 1972. DOI: 10.1021/ja00771a014 - "Dynamics of reactions in polar solvents. Semiclassical trajectory studies of electron-transfer and proton-transfer reactions", Arieh Warshel, J. Phys. Chem., 1982. DOI: 10.1021/j100209a016 - "Calculations of chemical processes in solutions", Arieh Warshel, J. Phys. Chem., 1979. DOI: 10.1021/j100475a014 - "Electrostatic basis of structure-function correlation in proteins", Arieh Warshel. Acc. Chem. Res., 1981. DOI: 10.1021/ar00069a004 - "Langevin Dipoles Model for ab Initio Calculations of Chemical Processes in Solution: Parametrization and Application to Hydration Free Energies of Neutral and Ionic Solutes and Conformational Analysis in Aqueous Solution", Jan Florián and Arieh Warshel, J. Phys. Chem. B, 1997. DOI: 10.1021/jp9705075 - "Protein Control of Redox Potentials of Iron-Sulfur Proteins", P. J. Stephens, D. R. Jollie, and A. Warshel, Chem. Rev., 1996. DOI: 10.1021/cr950045w
- "Energetics
and Dynamics of Enzymatic Reactions", Jordi
Villà and Arieh Warshel, J.
Phys. Chem. B, 2001. DOI: 10.1021/jp011048h
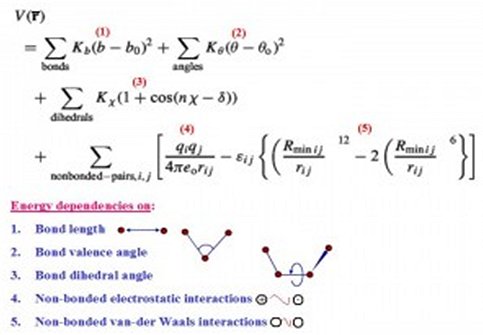
Εξίσωση για δύναμη πεδίου, ένα μοντέλο Υπολογιστικής Χημείας που χρησιμοποιεί απλούς όρους και παραμέτρους από πειραματικά δεδομένα για να υπολογίσει την ενέργεια ενός μορίου (εικόνα από τον Amit Kessel)
SCIENTIFIC AMERICAN 9/10/2013
Επιμέλεια κειμένου: Θανάσης Βαλαβανίδης, Καθηγητής 20/10/2013 |




 Στην
ανακοίνωση της Βασιλικής Σουηδικής Ακαδημίας εξηγεί τους λόγους για
τη βράβευση με το Βραβείο Νόμπελ Χημείας και αναφέρει:
Στην
ανακοίνωση της Βασιλικής Σουηδικής Ακαδημίας εξηγεί τους λόγους για
τη βράβευση με το Βραβείο Νόμπελ Χημείας και αναφέρει: