Λίστα "Χημικών Ενώσεων του Μήνα"
Η χημική ένωση του
μήνα
[Οκτώβριος 2009]
Επιμέλεια σελίδας:
Κων/νος Δημόπουλος, Καθηγητής -
Θανάσης Βαλαβανίδης, Καθηγητής
-
Κωνσταντίνος
Ευσταθίου, Καθηγητής
|
Φυσικoχημικές ιδιότητες:
[Αναφ. 1δ]
Εμφάνιση:
Λευκόχρωμη
ουσία, λιπαρής υφής.
Διαλυτή σε:
μεθανόλη, αιθανόλη, χλωροφόρμιο-μεθανόλη, χλωροφόρμιο:μεθανόλη:νερό
(1:1:0,9
v/v),
NaCl 0,15 M που περιέχει 1 mg/mL αλβουμίνης.
Αδιάλυτη σε:
χλωροφόρμιο, διαιθυλαιθέρα, βενζόλιο, ακετόνη, NaCl 0,15 M, νερό.
Κρίσιμη μικκυλιακή συγκέντρωση (critical
micelle
concentration,
CMC)
για τον
PAF
με 18 άτομα άνθρακα στην γλυκεριναιθερική αλυσίδα = 2
x
10-5 Μ.
Αντοχή σε διάφορα αντιδραστήρια:
Σταθερή
σε:
100ºC
για 1-3
h
/ σε HCl
4 Μ,
20ºC,
3
h
/ σε
NH3
0,5M,
20ºC,
1
h
/ σε οξικό ανυδρίτη, 60ºC,
1
h
/ σε υπεριωδικό οξύ 0,1 Μ,
20ºC,
2
h
/ NaNO3
0,25 Μ,
pH=5,6,
60ºC,
72 h.
Ασταθής
σε:
NaOH 0,5
M (υδατικό),
20ºC, 30 min /
NaOH
0,5
M (μεθανολικό), 2 min
/ Αιθερικό διάλυμα
LiAlΗ4,
32ºC,
22 min / HCl 6
M,
100ºC, 3
h
/ Οξικό οξύ: οξικός ανυδρίτης 2:1 (v/v),
150ºC, 16
h. |
 |
|
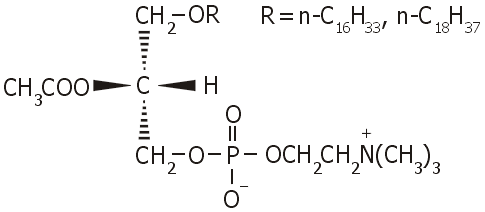
Παράγοντας Ενεργοποίησης
Αιμοπεταλίων
Platelet
Activating Factor
(PAF)
|
|
Τον Οκτώβριο του 2009
συμπληρώνονται ακριβώς 30 έτη από τη δημοσίευση της εργασίας
διευκρίνισης της δομής του PAF από ερευνητική ομάδα του
Πανεπιστημίου του Tέξας στο San Antonio. Στην ομάδα αυτή συμμετείχε,
ως μεταδιδακτορικός σπουδαστής,
ο Καθηγητής Βιοχημείας
του Τμήματος Χημείας, κ. Κων/νος Δημόπουλος, ο οποίος ανέλαβε την
κύρια επιμέλεια για την ιστοσελίδα αυτή |
|
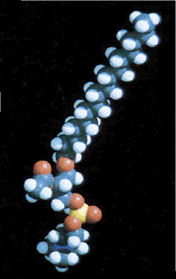 Συνοπτική
παρουσίαση του PAF Συνοπτική
παρουσίαση του PAF
 Ο
παράγοντας ενεργοποίησης αιμοπεταλίων
(Platelet
Activating Factor,
PAF)
αποτελεί λιποειδική ένωση που ανήκει στην τάξη των φωσφολιποειδών. Η ονομασία
της ένωσης κατα IUPAC
ως 1-Ο-αλκυλο-2-ακετυλο-sn-γλυκερο-3-φωσφο-χολίνη προσδιορίζει
δομικά την ένωση ως ένα γλυκεριναιθερικό ανάλογο της
φωσφατιδυλοχολίνης. Ο
παράγοντας ενεργοποίησης αιμοπεταλίων
(Platelet
Activating Factor,
PAF)
αποτελεί λιποειδική ένωση που ανήκει στην τάξη των φωσφολιποειδών. Η ονομασία
της ένωσης κατα IUPAC
ως 1-Ο-αλκυλο-2-ακετυλο-sn-γλυκερο-3-φωσφο-χολίνη προσδιορίζει
δομικά την ένωση ως ένα γλυκεριναιθερικό ανάλογο της
φωσφατιδυλοχολίνης.
Ο PAF είναι ένας πανίσχυρος ενεργοποιητής και μεσολαβητής πολλών λειτουργιών των
λευκών αιμοσφαιρίων. Προκαλεί συγκόλληση των αιμοπεταλίων, διαστολή των
αιμοφόρων αγγείων, ερεθισμό και αναφυλαξία. Επιπλέον, συμμετέχει στους
μηχανισμούς της αιμόστασης. Ακόμη και σε εξαιρετικά χαμηλές συγκεντρώσεις (της
τάξης των pM) ο PAF
προκαλεί επικίνδυνο ερεθισμό των αεραγωγών και έντονα συμπτώματα άσθματος [Αναφ.
1].
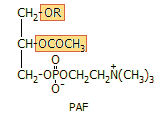
Από άποψη χημικής δομής ο PAF
διαθέτει δύο χαρακτηριστικά, τα οποία είναι σχετικώς ασυνήθιστα για τα
φωσφολιποειδή: (α) Στον άνθρακα C1 της γλυκερόλης (ή γλυκερίνης) υπάρχει
αιθερικός δεσμός (-CH2OR)
με ένα "μεγάλο" αλκύλιο κάτι το ασυνήθιστο, αφού ο
κανόνας είναι η ύπαρξη εστερικού δεσμού
(-CH2OCOR)
με "μεγάλα" λιπαρά οξέα, και (β) το υδροξύλιο του
άνθρακα C2 της γλυκερόλης είναι εστεροποιημένο με οξικό οξύ, (>CHOCOCH3),
κάτι το οποίο είναι επίσης ασυνήθιστο λόγω του μικρού μεγέθους του οξέος.
|
Ιστορική αναδρομή - Βιολογικές δράσεις
|
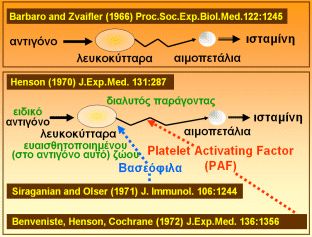
Σχήμα 1 |
Ενδείξεις
για την ύπαρξη αυτού του μορίου υπήρχαν από το 1966, όταν οι
Barbaro
και Zvaifler
παρατήρησαν ενεργοποίηση και συσσώρευση των
αιμοπεταλίων με ταυτόχρονη έκκριση ισταμίνης από αυτά μετά από επίδραση
αντιγόνου σε λευκοκύτταρα (λευκά αιμοσφαίρια) που βρίσκονται στο μικροπεριβάλλον
των αιμοπεταλίων
[Αναφ. 2].
Το 1970 ο Henson απέδειξε ότι η επίδραση
ειδικού αντιγόνου σε λευκοκύτταρα ζώου ευαισθητοποιημένου στο αντιγόνο αυτό,
προκαλεί την ελευθέρωση ενός διαλυτού παράγοντα, που προκαλεί έκκριση ισταμίνης
από τα αιμοπετάλια [Αναφ. 3].
Το 1971 οι
Siraganian
και
Olser
έδειξαν ότι ο παράγοντας αυτός δεν ελευθερώνεται από όλους τους τύπους
λευκοκυττάρων, αλλά μόνο από τα βασεόφιλα (περίπου το 1% των λευκοκυττάρων)
[Αναφ. 4].
|
Σχήμα
2 |
Το 1972 οι
Benveniste,
Henson και
Cochrane
ονόμασαν τον παράγοντα αυτό (με άγνωστη χημική δομή) παράγοντα
ενεργοποίησης των αιμοπεταλίων (Platelet-Activating
Factor,
PAF)
[Αναφ. 5] (Σχήμα 1).
Βιολογικη δράση του PAF
Το 1977 οι
Henson
και
Pinckard
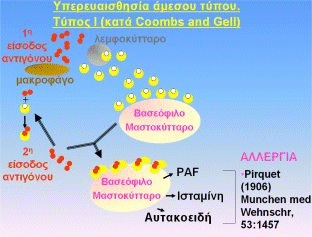
απέδειξαν ότι ο
PAF προκαλεί υπερευαισθησία άμεσου
τύπου (τύπος Ι κατά Coombs and
Gell ) μέσω της
παρατήρησης ότι τα επίπεδα του PAF στο αίμα αυξάνουν κατά την
IgE-αναφυλαξία, που αποτελεί μία μορφή
υπερευαισθησίας άμεσου τύπου (τύπος Ι)
[Αναφ. 6]. Με τον τρόπο
αυτό αποδείχθηκε ουσιαστικά ότι κατά τη δεύτερη είσοδο αντιγόνου σε οργανισμό
ευαισθητοποιημένο σε αυτό το αντιγόνο, συμβαίνουν εκτός από τις επωφελείς για
τον οργανισμό δράσεις και "άλλα-έργα" (εξ ου και "αλλεργία" από τον
Pirquet)
κατά τα οποία τα βασεόφιλα, όταν γεφυρωθούν τα αντισώματα που υπάρχουν στην
επιφάνειά τους με το ειδικό αντιγόνο, εκκρίνουν PAF, ισταμίνη και άλλες ενώσεις
που δρουν στο σημείο βιοσύνθεσής τους (αυτακοειδή)
[Σημείωση 1]. Διατυπώθηκε, μάλιστα, η άποψη ότι πρώτα εκλύεται ο
PAF,
ο οποίος στη συνέχεια προκαλεί την έκκριση της ισταμίνης και των άλλων
αυτακοειδών (Σχήμα 2).
Για πολλά χρόνια υπήρχε μια σύγχυση για το αν τα
παραπάνω συστατικά εκκρίνονται
ταυτόχρονα ή διαδοχικά και κυρίως αν πρώτα εκκρίνεται η ισταμίνη και στη
συνέχεια αυτή προκαλεί την έκκριση των άλλων. Το θέμα αυτό αν και δεν έχει γίνει
αποδεκτό από όλους, φαίνεται να έχει διαλευκανθεί και αναφέρεται παρακάτω. Το
1977 αποδείχθηκε ότι ο PAF εκκρίνεται κατά την τοπική αντίδραση
Arthus
και το 1979 έγινε από τον
Pinckard
η απομόνωση και
μελέτη του (άγνωστης έως τότε δομής ) PAF που
εκκρίνεται κατά την IgE-αναφυλαξία
[Αναφ. 7].
Από τις μελέτες αυτές θεωρήθηκε ότι ο PAF
είναι μια ένωση που μπορούσε να προκαλέσει ενεργοποίηση (συσσώρευση) των
αιμοπεταλίων μέσω μιας διαφορετικής οδού και άγνωστης έως τότε. Οι άλλες δύο
γνωστοί μέχρι τότε οδοί συσσώρευσης ήταν του αδενοσινοδιφωσφορικού οξέος
(ADP) και
του αραχιδονικού οξέος.


Σημείωση 1:
Τα
αυτακοείδη (autacoids) είναι βιολογικοί
παράγοντες που δρουν ως τοπικές ορμόνες, υφίστανται για περιορισμένο χρονικό
διάστημα και δεν μεταφέρονται μέσω της κυκλοφορίας αίματος. Χαρακτηρίζονται
κυρίως από τη δράση τους στους λείους μύες. Στους
αγγειακούς λείους μύες μπορούν να δράσουν ως αγγειοδιασταλτικά ή
αγγειοσυσταλτικά μέσα. Αγγειοδιασταλτικά αυτακοειδή απελευθερώνονται κατά την
άσκηση. Τυπικά αυτακοειδή είναι τα εικοσανοειδή, η αγγειοτενσίνη, το ΝΟ, η
ισταμίνη και η σεροτινίνη.
|
Βασικές γνώσεις για τα αιμοπετάλια
[Αναφ. 9]
 Γενικά:
Τα αιμοπετάλια (ή θρομβοκύτταρα) είναι θραύσματα κυττάρων του
αίματος που εμπλέκονται σε μηχανισμούς απαραίτητους για την πήξη του αίματος.
Χωρίς τον σχηματισμό θρόμβων (clots) αίματος κάθε διάρρηξη αιμοφόρου αγγείου θα
οδηγούσε σε αιμορραγία. Τα αιμοπετάλια χρειάζονται για να αποφευχθεί διαρροή
ερυθρών ερυθρών αιμοσφαιρίων ακόμη και από αγγεία που δεν έχουν υποστεί βλάβη. Γενικά:
Τα αιμοπετάλια (ή θρομβοκύτταρα) είναι θραύσματα κυττάρων του
αίματος που εμπλέκονται σε μηχανισμούς απαραίτητους για την πήξη του αίματος.
Χωρίς τον σχηματισμό θρόμβων (clots) αίματος κάθε διάρρηξη αιμοφόρου αγγείου θα
οδηγούσε σε αιμορραγία. Τα αιμοπετάλια χρειάζονται για να αποφευχθεί διαρροή
ερυθρών ερυθρών αιμοσφαιρίων ακόμη και από αγγεία που δεν έχουν υποστεί βλάβη.
|

'Ορος με
αιμοπετάλια έτοιμος για μετάγγιση. Διατηρούνται για πέντε ημέρες, σε
θερμοκρασία δωματίου με ελαφριά ανάδευση. |
Παραγωγή: Τα αιμοπετάλια παράγονται στον μυελό των οστών (περίπου 1011
ημερησίως), στα ονομαζόμενα μεγακαρυωτικά κύτταρα, τα οποία είναι
πολυπύρηνα κύτταρα. Η
θρομβοποιητίνη είναι μια ορμόνη που παράγεται κυρίως στο ήπαρ και
διεγείρει τον μηχανισμό παραγωγής αιμοπεταλίων. Η ορμόνη αυτή συνδέεται με τον
αριθμό των κυκλοφορούντων αιμοπεταλίων. Εάν ο αριθμός των αιμοπεταλίων είναι
ομαλός (150 έως 400 εκατομμύρια/mL αίματος), τα επίπεδα της θρομβοποιητίνης στον
ορό του αίματος παραμένουν χαμηλά. Εάν "πέσει" ο αριθμός των αιμοπεταλίων,
αυξάνονται τα επίπεδα της θρομβοποιητίνης στον ορό, έτσι ώστε να αυξηθεί η
παραγωγή αιμοπεταλίων.
Κυκλοφορία:
Η διάρκεια ζωής των κυκλοφορούντων στο αίμα αιμοπεταλίων είναι 7 έως 10 ημέρες.
Tα αιμοπετάλια δεσμεύονται και αδρανοποιούνται στον σπλήνα. Κακή λειτουργία του
σπλήνα (ή η απουσία του) μπορεί να αυξήσει τον αριθμό των αιμοπεταλίων.
Αντίθετα, υπερλειτουργία του σπλήνα μπορεί να οδηγήσει σε ταχύτερη καταστροφή
των αιμοπεταλίων και μείωση του αριθμού τους.
Λειτουργία: Τα
αιμοπετάλια ενεργοποιούνται όταν έρθουν
σε επαφή με
διάφορους παράγοντες όπως το κολλαγόνο ή τη θρομβίνη.
Μόλις ενεργοποιηθούν, το σχήμα τους αλλάζει (σχηματίζουν "ψευδόποδα"),
απελευθερώνουν
τα συστατικά των κοκκίων τους που περιλαμβάνουν για παράδειγμα πηκτικούς
παράγοντες κ.λπ.
Τα αιμοπετάλια
συγκολλούνται μεταξύ τους
(συσσωρεύονται) μέσω ειδικών υποδοχέων και επίσης προσκολλούνται σε άλλα
κύτταρα δημιουργώντας -σε συνδυασμό με το ινώδες (fibrin) ένα
"αιμοστατικό" βήσμα (plug) ή θρόμβο (clot).
Αριθμός αιμοπεταλίων κάτω από τα φυσιολογικά όρια οδηγεί σε ακατάσχετες
αιμορραγίες, ενώ αριθμός πάνω από τα φυσιολογικά όρια οδηγεί σε θρομβώσεις και
αποφράξεις αγγείων.

Μερικές από τις πολλές μορφές
με τις οποίες μπορούν να εμφανιστούν τα αιμοπετάλια (από
ιστοσελίδα του
Birmingham University) |
|
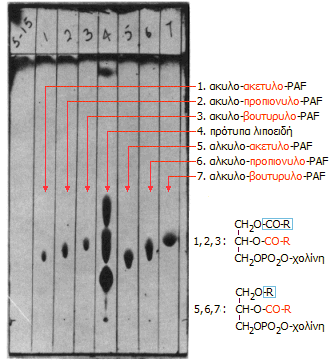
Χρωματογράφημα
λεπτής στιβάδας φωσφογλυκεριδίων με αλειφατικά οξέα μικρής αλυσίδας
(C2-C4) στη 2 θέση. 1-3: ακυλο-παράγωγα (εστερικά ανάλογα),
5-7: αλκυλο-παράγωγα (αιθερικά ανάλογα). Υπόστρωμα: Silica
gel, διαλύτης: CHCl3/CH3OH/H2O
(65:35:6), εμφάνιση: απανθράκωση με π.Η2SO4
[Αναφ. 8]. |
Σύνθεση PAF και αναλόγων
Τον Οκτώβριο του 1979 διαλευκάνθηκε και
αποδείχθηκε η δομή του PAF από τους Demopoulos, Pinckard και
Hanahan,
στο Πανεπιστήμιο του Τέξας στο
San Antonio.
Διαπιστώθηκε ότι ο
PAF είναι μια σχετικά απλή
ένωση, ένα φωσφολιποειδές με δομή 1-Ο-αλκυλο-2-ακετυλο-sn-γλυκερο-3-φωσφοχολίνη
[Αναφ. 8].
Σημαντικό
ρόλο για τη βιολογική δράση του
PAF
διαδραματίζει η ακετυλομάδα της
sn-2 θέσης του σκελετού της γλυκερόλης, καθώς η απομάκρυνσή της οδηγεί σε
απώλεια της βιολογικής δραστικότητας.
Επιπλέον,
στην ίδια δημοσίευση επιβεβαιώνεται η δομή του PAF μέσω της ημισυνθετικής
παρασκευής του και με πρόδρομη ένωση το
λιποειδές 1-Ο-αλκυλο-2-ακυλο-sn-γλυκερο-3-φωσφο-χολίνη, ένα
γλυκεριναιθερικό ανάλογο της φωσφατιδυλο-χολίνης, συστατικό των μεμβρανών των
κυττάρων της καρδιάς του βοός,
σύμφωνα με την ακόλουθη αλληλουχία αντιδράσεων:
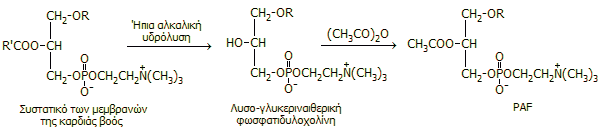
Με ήπια αλκαλική υδρόλυση απομακρύνεται το λιπαρό
οξύ R'COOH της sn-2 θέσης της πρόδρομης και σχηματίζεται η αντίστοιχη
λυσο-γλυκεριναιθερική φωσφατιδυλοχολίνη. Στη συνέχεια ακολουθεί
ακετυλίωση με οξικό ανυδρίτη του ελεύθερου υδροξυλίου που οδηγεί
στο επιθυμητό προϊόν του
PAF. 'Ετσι,
αποφεύγεται η πολύ δύσκολη ολική χημική σύνθεση ενός
sn-γλυκερο-3-φωσφο-λιποειδούς
[Σημείωση 2].
Η μέθοδος αυτή λόγω των πλεονεκτημάτων της χρησιμοποιείται και για την εμπορική
παρασκευή του
PAF
από πολλές εταιρείες (SIGMA,
SUPELCO).
Εδώ θα πρέπει να τονισθεί ότι ο PAF διαθέτει ένα ασύμμετρο άτομο άνθρακα (ο C2
της γλυκερόλης) και από τις δύο εναντιομερείς μορφές μόνο η L-μορφή είναι η
βιολογικώς δραστική, ενώ η
D-μορφή
δεν παρουσιάζει καμία βιολογική δράση
[Σημείωση 3].
Ο συνθετικά
παρασκευασμένος PAF έχει όλες τις χημικές και βιολογικές ιδιότητες του
PAF φυσικής προέλευσης.
Στην πραγματικότητα συντέθηκαν διάφορα
ανάλογα του
PAF. Στην
πλάκα της χρωματογραφία λεπτής στιβάδας φαίνεται η χρωματογραφική συμπεριφορά
μερικών συνθετικών αναλόγων του PAF.
|
Σχήμα
3 |
Σχέση
δομής - δραστικότητας. Διαπιστώθηκε ότι τα
εστερικά ανάλογα του PAF είχαν βιολογική δραστικότητα μικρότερη κατά τρεις
τάξεις μεγέθους από τα αντίστοιχα
αιθερικά ανάλογα. Επίσης, διαπιστώθηκε ότι η αντικατάσταση του οξικού
οξέος στην
sn-2 θέση του σκελετού γλυκερόλης, με
οξέα με ανθρακική αλυσίδα μεγαλύτερη των 4 ατόμων άνθρακα στερούσε στην ένωση τη
βιολογική της δράση.
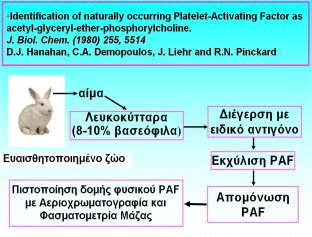
Το 1980
αποδείχθηκε
από την ομάδα του San Antonio η
δομή του φυσικής προέλευσης μορίου του
PAF.
Μια ποσότητα (της τάξης μερικών μg)
φυσικού PAF
παρασκευάστηκε με τη
χρήση εκατοντάδων κουνελιών, τα οποία είχαν ευαισθητοποιηθεί σε ειδικό αντιγόνο
και μετά από επίπονη εργασία αρκετών μηνών. Από τα ζώα αυτά λαμβανόταν αίμα από
το οποίο διαχωρίζονταν τα λευκοκύτταρα, τα οποία στη συνέχεια διεγείρονταν με το
ειδικό αντιγόνο. Ο
PAF που
εκκρινόταν με αυτόν τον τρόπο εκχυλίστηκε, καθαρίστηκε και διαπιστώθηκε ότι η
δομή του ταυτίζεται με τη δομή του συνθετικού
PAF.
Συγκεκριμένα, επειδή δεν υπήρχαν τότε τα σύγχρονα μέσα προσδιορισμού της δομής,
η ουσία διασπάστηκε υδρολυτικά στα επιμέρους συστατικά της, τα οποία στη
συνέχεια μετατράπηκαν σε πτητικά παράγωγα και ταυτοποιήθηκαν με
αεριοχρωματογραφία (GC), με φασματοσκοπία μαζών (MS),
όπως και με συνδυασμό και των δύο τεχνικών (GC/MS)
(Σχήμα 3).
'Ετσι αποδείχτηκε η ύπαρξη αιθερικού δεσμού με ανθρακική αλυσίδα 16 και 18
ατόμων άνθρακα, οξικού οξέος, φωσφορικής ομάδας και χολίνης. Η όλη διεργασία
γινόταν παράλληλα και στον PAF φυσικής προέλευσης,
αλλά
και σε μοριακά ανάλογα του συνθετικού
PAF
και τα αποτελέσματα συγκρίνονταν για επιβεβαίωση. Το μοριακό βάρος του
PAF φυσικής
προέλευσης
προσδιορίστηκε από τη μάζα του μοριακού ιόντος (mass ion number),
που λήφθηκε από φυσικό
PAF
και από τα διάφορα μοριακά ανάλογα του συνθετικού
PAF
με την καλύτερη τότε διαθέσιμη τεχνική, τη
φασματοσκοπίας μαζών εκρόφησης μέσω πεδίου (field
desorption mass spectrometry)
[Σημείωση 4]. Με τον τρόπο αυτό αποδείχτηκε
-πέρα από κάθε αμφιβολία- ότι ο φυσικής προέλευσης
PAF
ήταν μίγμα ενώσεων με ανθρακική αλυσίδα 16 και 18 ατόμων άνθρακα στην sn-1
θέση του σκελετού της γλυκερόλης, οξικό οξύ στην sn-2 θέση και
φωσφο-χολίνη στην sn-3 θέση
[Αναφ. 10].


 Σημείωση
2:
Το πρόθημα λυσο- στα γλυκερίδια, δηλώνει την παρουσία ελεύθερου
γλυκερινικού υδροξυλίου.
Σημείωση
2:
Το πρόθημα λυσο- στα γλυκερίδια, δηλώνει την παρουσία ελεύθερου
γλυκερινικού υδροξυλίου.
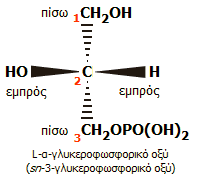
Σημείωση 3:
Επεξήγηση του sn-: Στα παράγωγα της γλυκερόλης (τριγλυκερίδια,
φωσφολιποειδή κ.λπ.), εάν τα δύο α-ΟΗ (πρωτοταγή υδροξύλια) της γλυκερόλης
συνδεθούν με διαφορετικές ομάδες, τότε το άτομο άνθρακα στη 2η θέση (άνθρακας
C2) καθίσταται "ασύμμετρο". Πολλά ένζυμα που δρουν στα λιποειδή, διαφoρoπoιoύν
τη δράση τους έναντι των δύο δυνατών εναντιομερών μορφών, επομένως η
στερεοχημεία των ενώσεων αυτών είναι κρίσιμη και πρέπει να υποδηλώνεται στην
ονομασία τους. Στο σύστημα στερεoειδικής αρίθμησης (stereospecific
numbering, sn-) χρησιμοποιείται για την περιγραφή των εναντιομερών
παραγώγων της γλυκερόλης.
Σύμφωνα με το σύστημα sn, οι
άνθρακες της γλυκερόλης απαριθμούνται (από 1 έως 3), από πάνω προς τα κάτω, έτσι
ώστε με τον "ασύμμετρο" άνθρακα (C2) στο επίπεδο του κειμένου, το δευτεροταγές
υδροξύλιο (ελεύθερο ή μη) ευρίσκεται πάντοτε εμπρός αριστερά. Στο σχήμα
(αριστερά) δείχνεται η διάταξη στο χώρο του L-α-γλυκεροφωσφορικού οξέος, το
οποίο θα πρέπει να ονομαστεί sn-3-γλυκεροφωσφορικό οξύ. Είναι προφανές,
ότι ο οπτικός αντίποδάς του, το D-α-γλυκεροφωσφορικό οξύ θα πρέπει να ονομαστεί
sn-1-γλυκεροφωσφορικό οξύ.
Σημείωση 4:
Με τον όρο φασματοσκοπία μαζών εκρόφησης μέσω πεδίου, περιγράφεται τύπος
φασματοσκοπίας μαζών κατά την οποία ο σχηματισμός ιόντων ενός υλικού σε αέρια
φάση, προκύπτει με επίδραση ισχυρού ηλεκτρικού πεδίου σε στερεή επιφάνεια
(γνωστή ως "εκπομπός"), στην οποία έχει αποτεθεί μικρή ποσότητα του εξεταζόμενου
υλικού. Ωστόσο, ο όρος "εκρόφηση μέσω πεδίου" δεν είναι απολύτως ορθός διότι
υπονοεί ότι το υλικό εκροφάται από τον εκπομπό ως ιόν υπό την επίδραση του
ηλεκτρικού πεδίου. Υπάρχουν αυξανόμενες ενδείξεις ότι αρκετά από τα ιόντα
σχηματίζονται λόγω θερμικού ιοντισμού και αρκετά με ιοντισμό του ατμού του
υλικού. Ο ιοντισμός του υλικού είναι πρακτικά μηδενικός, εάν ο εκπομπός δεν
θερμανθεί με ηλεκτρικό ρεύμα.
Αντίκτυπος από τη διευκρίνιση της δομής του
PAF
|

Οι καθηγητές
Hanahan (αριστερά) και
Pinckard (δεξιά) σε
δημοσίευση της τοπικής εφημερίδας
San
Antonio Light (31/10/1979) |
Μερικές εβδομάδες μετά τη
δημοσίευση της δομή του
PAF
στο
J.
Biol.
Chem.
(1979), δημοσιεύτηκε η εργασία «Antihypertensive
activity of an alkyl-ether
analog of phosphatidyl-choline»
των
Blank,
Snyder,
Byers,
Brooks
και
Muirhead
[Αναφ. 11].
Η εργασία αυτή προέκυψε από τη μελέτη εκχυλισμάτων
νεφρικών τμημάτων, όπου παρατηρήθηκε η ύπαρξη ενός δραστικού
λιποειδούς, στο οποίο δόθηκε η ονομασία
Αντιυπερτασικό Πολικό Λιποειδές του Μυελού των Νεφρών
(Antihypertensive
Polar Renomedullary Lipid,
APRL).
Στη μελέτη αυτή έγινε σύνθεση διαφόρων λιποειδών μεταξύ των
οποίων και του
PAF,
ο οποίος βρέθηκε να έχει δράση
ανάλογη με το
APRL.
Στα επόμενα χρόνια διαπιστώθηκε ότι ο
PAF
έχει και αντι-υπερτασική δράση και ότι ταυτίζεται με το
λιποειδές που ονόμαζαν
APRL.
Μερικούς μήνες μετά τη
δημοσίευση για τη δομή του
PAF,
οι
J.
Benveniste,
M.
Tence,
P.
Varenne,
J.
Bidault,
C.
Boullet,
J.
Polonsky
έκαναν στο Παρίσι την ανακοίνωση "Semi-synthese
et structure proposee du facteur activant les plaquettes
(PAF).
Un alkyl-ether
analogue de la lysophosphatidyl-choline",
που δημοσιεύτηκε στα Πρακτικά της Ακαδημίας των Επιστημών
στο Παρίσι,
Compt.
Rend.
Acad.
Sci.
Paris
(Series
D)
289:1037 (1979) ως πρόδρομη δημοσίευση με μικρό πειραματικό
μέρος, όπου παρουσιάζονταν τα αποτελέσματα για μια ένωση με
τη δομή που είχε ήδη δημοσιευτεί στο
J.
Biol.
Chem.
και είχε δράση ανάλογη του
PAF.
Η ανακάλυψη της δομής του
PAF
αποτέλεσε είδηση που προβλήθηκε από την τηλεόραση αρχικά σε
τοπικό επίπεδο πολιτείας (Τέξας) και στη συνέχεια σε εθνικό
(ομοσπονδιακό) επίπεδο των ΗΠΑ. Στη φωτογραφία είναι το
πρωτοσέλιδο της τοπικής εφημερίδας που αναφέρεται στη
σημασία της ανακάλυψης του
PAF
για τις αλλεργίες, όπου εμφανίζονται και οι δύο καθηγητές
-Διευθυντές των Τμημάτων
(Βιοχημείας και Παθολογίας) στα οποία διεξήχθη η
έρευνα.
Η ανακάλυψη του
PAF
απετέλεσε θέμα έγκυρων επιστημονικών περιοδικών όπως του
Nature
στο
"News
and Views",
αλλά και κύριο άρθρο (Editorial)
από τον
συντάκτη του περιοδικού αυτού
[Αναφ. 12].
Αναφέρεται ακόμα ένα κύριο άρθρο που γράφτηκε πολλά χρόνια
μετά (2000) στο περιοδικό
European Journal Of Lipid
Science and Technology
[Αναφ. 13].
Η διαλεύκανση της δομής του
PAF
άνοιξε νέους ορίζοντες στην έρευνα των λιποειδών και κυρίως
των φωσφολιποειδών και των γλυκεριναιθερικών λιποειδών, αφού
ήταν το πρώτο βιολογικά δραστικό φωσφολιποειδές που δρούσε
ως αγωνιστής. Βεβαίως έδωσε σημαντική ώθηση και στην
έρευνα του
PAF
με αποτέλεσμα να διοργανώνονται κάθε 3 χρόνια Παγκόσμια
Συνέδρια
με αποκλειστικό θέμα τον
PAF.
Μετά από 24 χρόνια (8 Συνέδρια: Paris, 1983 - Gatlinburg,
Tennessee, 1986 - Tokyo, 1989 - Snowbird, Utah, 1992 -
Berlin, 1995 - New Orleans, 1998 - Tokyo, 2001 - Berlin,
2004) η έρευνα στο θέμα του
PAF
είχε επεκταθεί σε τόσους τομείς της επιστήμης, ώστε έπαψε να
αποτελεί θέμα ενός Συνεδρίου και ενσωματώθηκε στα επιμέρους
ειδικά συνέδρια. Στην Ελλάδα έγιναν τρία Πανελλήνια Συνέδρια
με θέμα τον
PAF (Ιωάννινα, 1987 -
Αθήνα, 1990 - Ιωάννινα, 1994)
[Αναφ. 1α].
|
|

Σχήμα 4 |
Σύγκριση βιολογικών ιδιοτήτων συνθετικού και
φυσικού PAF
Μετά τη διαλεύκανση της χημική δομής
του
PAF
και την απόδειξη ότι
in vitro
οι βιολογικές ιδιότητες
του συνθετικού και του φυσικού μορίου ταυτίζονται, εξετάστηκε εάν αυτό ισχύει
και για τις ιδιότητες του συνθετικού και φυσικού μορίου in vivo. Για τον
λόγο αυτό
χορηγήθηκε σε κουνέλια το ειδικό αντιγόνο στο οποίο είχαν ευαισθητοποιηθεί,
δηλαδή προκλήθηκε IgE
αναφυλαξία, κατά την οποία ο οργανισμός του ζώου παράγει
PAF.
Σε άλλη ομάδα ζώων χορηγήθηκε ο φυσικός
PAF
και σε μια τρίτη ομάδα ο συνθετικός
PAF.
Και στις τρείς περιπτώσεις προκλήθηκε πανομοιότυπο αλλεργικό σοκ, με συσσώρευση
των αιμοπεταλίων κυρίως στους πνεύμονες.
Στην περίπτωση του
συνθετικού
PAF, όπου υπήρχε η
δυνατότητα ποσοτικής μέτρησης του χορηγούμενου
PAF,
προκλήθηκε θάνατος των πειραματόζωων σε χρόνο 2
min
μετά από χορήγηση 2,4 μg
PAF
[Αναφ. 14α].
Επίσης,
σε πειράματα τόσο σε
κουνέλια όσο και σε κυνοπίθηκους (βαβουίνους), αποδείχθηκε ότι ο συνθετικός
PAF
προκαλεί τα ίδια αγγειακά-καρδιαγγειακά-αναπνευστικά προβλήματα με την
αναφυλαξία
[Αναφ. 14β, 14γ].
Τα αποτελέσματα αυτά προέκυψαν και όταν ο
PAF
χορηγήθηκε σε κουνέλια στα οποία είχαν απομακρυνθεί τα αιμοπετάλιά τους
[Αναφ. 14δ],
δηλαδή αποδείχθηκε ότι η δράση του
PAF
δεν ασκείται μόνο μέσω της επίδρασής του στα αιμοπετάλια, αλλά ότι έχει άμεση
επίδραση σε κύτταρα και ιστούς, ανοίγοντας έτσι ένα νέο μεγάλο κεφάλαιο στην
έρευνα του
PAF
(Σχήμα 4).
Στη συνέχεια τα
πειράματα επεκτάθηκαν και σε ανθρώπους. Τα μέλη της ερευνητικής ομάδας του
San Antonio έλαβαν με υποδόρια ένεση
52 μg
συνθετικού PAF,
οπότε προκλήθηκε σε χρόνο 5 min δερματική αντίδραση με τοπικό πόνο, κνησμό και
οίδημα με ερύθημα. Τα παραπάνω φαινόμενα δεν αναστέλλονταν αν είχε προηγηθεί στο
άτομο χορήγηση αντισταμινικών (Hydroxyzine)
ή καρτιζονούχων (Prednisone)
ή τέλος ασπιρίνης ή ινδομεθακίνης. Δηλαδή, o
PAF
ασκούσε τη δράση του μέσω διαφορετικών οδών από αυτές που ανέστελλαν τα παραπάνω
φάρμακα, φανερώνοντας
-για πρώτη φορά παγκοσμίως-
την έλλειψη φαρμάκου κατάλληλου για την πλήρη
αντιμετώπιση των αλλεργικών φαινομένων
[Αναφ. 15].
Επίσης, αποδείκνυε ότι στη δερματική τοπική αλλεργική αντίδραση η ισταμίνη δεν
αποτελούσε τον πρωταρχικό παράγοντα.
Σήμερα γνωρίζουμε ότι η ισταμίνη μπορεί να προκαλέσει
έκκριση
PAF,
όπως ότι και ο
PAF
μπορεί να προκαλέσει έκκριση ισταμίνης. Πρωτεύοντα όμως ρόλο στα αλλεργικά
φαινόμενα παίζει ο
PAF, ο
οποίος εκκρίνεται πρώτος και δρα άμεσα στα διάφορα κύτταρα και δευτερογενώς
προκαλεί την έκκριση ισταμίνης και άλλων αυτακοειδών, που ενισχύουν και
διατηρούν το φαινόμενο.
Η άποψη αυτή
έχει επιβεβαιωθεί από
πολλά πειραματικά δεδομένα πολλών
ερευνητών. Ενδεικτικά αναφέρονται δύο πρόσφατες εργασίες: α) Του
Vadas et al.
(2008), σύμφωνα με την οποία τα επίπεδα του
PAF
σχετίζονται στατιστικά με τη βαρύτητα των συμπτωμάτων σε οξείες αλλεργικές
αντιδράσεις, ενώ αυτό δεν συμβαίνει με την ισταμίνη [Αναφ.
16]
και β) του
Shibamoto et al.
(2008), σύμφωνα με την οποία
στην αναφυλαξία στα ποντίκια συμμετέχει
κυρίως ο
PAF
και όχι η ισταμίνη [Αναφ. 17].
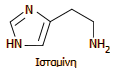 Δυο
λόγια για την ισταμίνη Δυο
λόγια για την ισταμίνη
Η ισταμίνη είναι
μια βιογενής αμίνη, προϊόν αποκαρβοξυλίωσης του αμινοξέος
ιστιδίνη. Εμπλέκεται στους τοπικούς μηχανισμούς
ανοσοαπόκρισης και επιπλέον δρα ως νευροδιαβιβαστής. Η
ισταμίνη διεγείρει τους μηχανισμούς φλεγμονώδους
απόκρισης. Ιστιδίνη παράγεται, κατά την ανοσοαπόκριση σε
παθογόνους εισβολείς, από τα βασεόφιλα και τα σιτευτικά
κύτταρα (mast cells) των παρακείμενων συνδετικών ιστών. Η
ισταμίνη αυξάνει τη διαπερατότητα των τριχοειδών αγγείων από
τα λευκά αιμοσφαίρια, διευκολύνοντας την "επίθεσή" τους κατά
των παθογόνων εισβολέων
|
Ο
PAF
είναι ο ισχυρότερος σήμερα γνωστός φλεγμονώδης παράγοντας:
In
vivo, σε κουνέλια, για
θετικό αποτέλεσμα σε αναφυλακτικό σοκ, η δραστική του συγκέντρωση είναι της
τάξης των 0,1 nM και σε συγκεντρώσεις της τάξης 10 nM επιφέρει τον θάνατο.
In vitro,
σε πλυμένα αιμοπετάλια κουνελιού, για συσσώρευση (με 50% έκκριση των δραστικών
συστατικών) απαιτούνται: 0,01 ng
PAF, 10
ng
ADP, 10
ng
θρομβίνης, 4 μg
αραχιδονικού οξέος (πρόδρομη ένωση βιολογικώς δραστικών ενώσεων, όπως π.χ. οι
προσταγλαδίνες) ή 10 μg
κολλαγόνου.
|

Η διάταξη
συσσωρευματόμετρου (Εργαστήριο Βιοχημείας, Τμήματος Χημείας του
Πανεπιστημίου Αθηνών) |
Ανίχνευση και προσδιορισμός του PAF
Λόγω της ισχυρής βιολογικής δράσης του PAF, υπάρχει σε ελάχιστες συγκεντρώσεις
στο αίμα (pM
έως
nM)
γεγονός που καθιστά
εξαιρετικά δύσκολη
τη χημική του ανίχνευση και τον ποσοτικό προσδιορισμό του. Για τον λόγο αυτό
έχουν αναπτυχθεί βιολογικές μέθοδοι ανίχνευσης και προσδιορισμού του, που κυρίως
βασίζονται στην ιδιότητά του να προκαλεί συσσώρευση σε αιμοπετάλια που
παρακολουθείται φωτομετρικά. Για να είναι όμως αξιόπιστα τα αποτελέσματα της
βιολογικής δοκιμασίας απαιτείται πολύ καλός χημικός διαχωρισμός του από τις
άλλες ενώσεις με χρωματογραφικές μεθόδους.
Συσσωρευματόμετρο (aggregometer):
Είναι ένα τροποποιημένο φωτόμετρο, με κυψελίδα χωρητικότητας 0,5 ή 0,25 mL,
θερμοστατούμενη στους 37ºC και αναδευόμενη από μικρό μαγνητικό αναδευτήρα στις
1200 rpm.
Τυπική διαδικασία μέτρησης: Αρχικά προστίθεται το
εναιώρημα των αιμοπεταλίων σε πλάσμα αίματος ("πλάσμα πλούσιο σε αιμοπετάλια") ή
σε κατάλληλο διάλυμα ("πλυμένα αιμοπετάλια"). Στη φάση αυτή διέρχεται κάποιο
ποσοστό της φωτεινής δέσμης και η διαπερατότητα αυτή καταγράφεται με τη μορφή
σταθερής ταλάντωσης καμπύλης σε διάγραμμα % διαπερατότητας ως προς τον χρόνο. 'Οταν
στη συνέχεια προστεθεί ο συσσωρευτικός παράγοντας, τότε κατά το πρώτο στάδιο του
φαινομένου της συσσώρευσης όπου επέρχεται αλλαγή σχήματος και διόγκωση των
αιμοπεταλίων, η διαπερατότητα μειώνεται και το καταγραφικό δίνει καμπύλη
μικρότερης ταλάντωσης που κινείται προς τα κάτω.
Στη συνέχεια, κατά το δεύτερο στάδιο του φαινομένου
της συσσώρευσης όπου σχηματίζονται θρόμβοι από συσσωρευμένα αιμοπετάλια, η
διαπερατότητα αυξάνεται και το καταγραφικό δίνει καμπύλη που κινείται προς τα
άνω, με συνεχώς μεγαλύτερη ταλάντωση (θόρυβο), ανάλογα με το μέγεθος των
σχηματιζόμενων θρόμβων. Αν η συγκέντρωση του συσσωρευτικού μέσου δεν είναι πολύ
μεγάλη, ακολουθεί και τρίτο στάδιο κατά το οποίο επέρχεται αποσυσσώρευση των
αιμοπεταλίων και επαναφορά τους στην αρχική τους κατάσταση, οπότε η καμπύλη στο
καταγραφικό κινείται προς τα κάτω με συνεχώς μικρότερη ταλάντωση και καταλήγει
στην αρχική της μορφή και περίπου στο αρχικό επίπεδο της % διαπερατότητας. Η
τυπική μέτρηση διαρκεί από 3 έως 6 min.
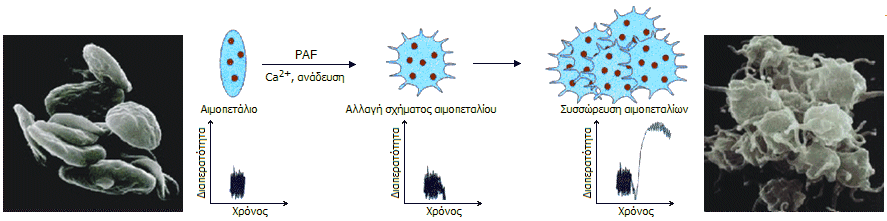
Αρχή μεθόδου βιολογικής μεθόδου προσδιορισμού του
PAF. Στις φωτογραφίες δείχνεται η μορφή αιματοπεταλίων
στη φυσιολογική τους κατάσταση (αριστερά) και των αιμοπεταλίων μετά την επίδραση
του PAF.
Φυσιολογικές δράσεις του PAF
Ο
PAF
διαδραματίζει κεντρικό ρόλο σε πολλές
βιοχημικές διαδικασίες παθολογικές ή μη. Βιοσυντίθεται από πολλούς τύπους
κυττάρων, από κύτταρα προκαρυωτικά και ευκαρυωτικά, από φυτικά-ζωικά κύτταρα,
αλλά και από ιστούς.
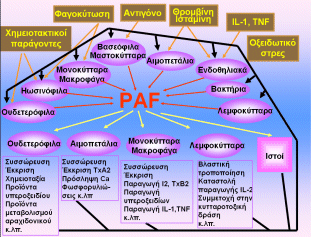
Παρουσιάζει πληθώρα δράσεων και εμπλέκεται σε μεγάλο
αριθμό παθοφυσιολογικών καταστάσεων. Ακολουθεί
συνοπτική παρουσίαση [Αναφ. 1α]:
|
Kύτταρα
που παράγουν
PAF:
Βασεόφιλα (κουνελιού, ανθρώπου).
Πολυμορφοπύρηνα, ουδετερόφιλα (κουνελιού, ανθρώπου, χοίρου). Μακροφάγα
(περιτοναϊκά ποντικού, ανθρώπου). Κυψελιδικά (αρουραίου, κουνελιού, πιθήκου,
ανθρώπου). Μονοκύτταρα (ανθρώπου). Μαστοκύτταρα μυελού οστών (ποντικού),
πνεύμονα (ανθρώπου). Ηωσινόφιλα (κουνελιού, ανθρώπου). Αιμοπετάλια (κουνελιού,
ανθρώπου). Ενδοθηλιακά κύτταρα (Καλλιέργειες ενδοθηλιακών κυττάρων κουνελιού,
ανθρώπου). Νεφρικά κύτταρα (Απομονωμένα κύτταρα μυελού του νεφρού αρουραίου,
απομονωμένα σπειράματα αρουραίου, καλλιέργειες μεσαγγειακών κυττάρων).
Πρωτόζωα
(Tetrahymena pyriformis).
Μύκητες
(Saccharomyces cerevisiae).
Προκαρυωτικά κύτταρα
(βακτήρια).
Φυτικά κύτταρα
(Urtica
dioica). |
|
Δράσεις του
PAF σε κύτταρα στόχους:
Πολυμορφοπύρηνα,
Ουδετερόφιλα: Αποκοκκίωση - Συσσώρευση - Χημειοταξία - Παραγωγή προϊόντων
υπεροξειδίου - Aύξηση της προσκολλητικής ικανότητας (στα ενδοθηλιακά κύτταρα και
σε ξένες επιφάνειες) - Ενεργοποίηση της παραγωγής προϊόντων μεταβολισμού του
αραχιδονικού οξέος.
Ηωσινόφιλα: Χημειοταξία - 'Εκκριση
κατιονικών πρωτεϊνών - Αύξηση κυτταροτοξικότητας - Σύνθεση LT-C4 - Παραγωγή
προϊόντων υπεροξειδίου - Αύξηση συγκέντρωσης ελευθέρων ιόντων Ca2+.
Μονοκύτταρα-Μακροφάγα:
Συσσώρευση - 'Εκκριση άλλων μεσολαβητών - Αύξηση παραγωγής προστακυκλίνης Ι2 και
TxB2 - Παραγωγή υπεροξειδίων - Παραγωγή ΙL-1 - Επίδραση στα επίπεδα c-AMP -
Eνεργοποίηση κύκλου φωσφατιδυλοϊνοσίτη
Ενδοθηλιακά: Αύξηση
ενδοκυττάριου Ca2+ - Ανακατανομή κυτταροσκελετού - Σύνθεση
προστακυκλίνης
Λεμφοκύτταρα: Βλαστική
τροποποίηση - Καταστολή παραγωγής IL-2 - Συμμετοχή στην κυτταροτοξική δράση
Αιμοπετάλια: Αποκοκκίωση -
Συσσώρευση - Αλλαγή σχήματος - Αύξηση της εισροής Ca2+ - Ενεργοποίηση
του κύκλου του φωσφατιδυλοϊνοσίτη και της παραγωγής προϊόντων μεταβολισμού του
αραχιδονικού οξέος - Φωσφορυλίωση πρωτεϊνών
Πρωτόζωα (Tetrahymena pyriformis): Eνεργοποίηση της παραγωγής προϊόντων μεταβολισμού του αραχιδονικού
οξέος - Αύξηση της γλυκογονόλυσης - Μεταβολισμός της σύστασης των λιποειδών
Φυτά: Επίδραση στο σύστημα
των μικροσωμάτων - Επίδραση στη μεμβράνη των θυλακοειδών των χλωροπλαστών
|
|
Δράσεις του
PAF
σε παρασκευάσματα ιστών και
σε μεμονωμένα όργανα:
'Ηπαρ: Αυξάνει την
ηπατική γλυκογονόλυση
Λείες μυϊκές ίνες:
Προκαλεί σύσπαση των λείων μυϊκών ινών σε απομονωμένο ειλεό μέσω ειδικού
υποδοχέα.
Πνευμονικός ιστός:
Προκαλεί μείωση της επιφάνειας των τριχοειδών, σύσπαση του απομονωμένου
πνευμονικού ιστού (με άμεση δράση στα συσταλτά κύτταρα) και μείωση της
διατασιμότητας αυτού, καθώς επίσης και αγγειοσύσπαση.
Καρδιά: Σε
απομονωμένη καρδιά προκαλεί μείωση της συσταλτικής ικανότητας της
κοιλίας, σύσπαση των στεφανιαίων (άμεση δράση) με αποτέλεσμα τη μεγάλη
μείωση της ροής του αίματος και την πρόκληση αρρυθμίας αγωγιμότητας - Σε
απομονωμένο θηλοειδή μυ καρδιάς προκαλεί παροδική θετική ινότροπη και
σημαντική αρνητική δρομότροπη δράση.
Νεφρός: Σε
κυτταροκαλλιέργειες μεσαγγειακών κυττάρων προκαλεί σύσπαση και αλλαγή
σχήματος (με αποτέλεσμα την μείωση του μεγέθους των σπειραμάτων) -
Έκκριση ελευθέρων ριζών και ενεργοποίηση σύνθεσης προσταγλανδινών - Σε
απομονωμένα σπειράματα προκαλεί μείωση της διατομής τους (με αποτέλεσμα
την τροποποίηση της σπειραματικής διήθησης). |
|
Δράσεις του PAF
in vivo:
Βροχόσπασμος (χωρίς
μεσολάβησης ισταμίνης ή σεροτονίνης) - Θρομβοπενία - Ουδετεροπενία -
Βασεοπενία
Αναφυλακτικές
αντιδράσεις:
Στο αναπνευστικό: Μείωση αναπνευστικής συχνότητας (με περιόδους
άπνοιας λόγω καταστολής του αντίστοιχου κέντρου) - Βρογχόσπασμο - Αύξηση
των πνευμονικών αντιστάσεων - Μείωση της ενδοτικότητας του πνεύμονα -
Αύξηση της πίεσης στις πνευμονικες αρτηρίες με
αποτέλεσμα πρόκληση πνευμονικού οιδήματος. Στο κυκλοφορικό:
Σχεδόν άμεση αλλαγή του ηλεκτροκαρδιογραφήματος (αρχικά παροδική βραδυκαρδία
και μετά ταχυκαρδία με αρρυθμία αγωγιμότητας και πτώση της ανάσπασης) - Αιμοδυναμικές
αλλαγές: 1) μείωση της συστολικής πίεσης της αριστερής
κοιλίας, 2) μείωση της συστολικής και της διαστολικής αρτηριακής
πίεσης στις μηριαίες που στη συνέχεια παροδικά αυξάνουν και
μειώνονται, 3) αύξηση της κεντρικής φλεβικής πίεσης, 4) αύξηση
της πίεσης στο δεξιό κόλπο, 5) μείωση της τελοδιαστολικής πίεσης
στη δεξιά κοιλία (με αποτέλεσμα τη μείωση της πλήρωσης της
αριστερής κοιλίας και μείωση του καρδιακού παλμού)
Επίδραση στη
συστηματική κυκλοφορία:
Μείωση της μέσης
αρτηριακής πίεσης (με αποτέλεσμα την πρόκληση
shock, λόγω της μείωσης του κυκλοφορούντος όγκου αίματος
εξαιτίας της εξαγγείωσης και της αύξησης της περιφερειακής
αποθήκης) - Μείωση του κατά λεπτό όγκου αίματος - Μείωση των
περιφερειακών αντιστάσεων
Επίδραση στο
πεπτικό σύστημα:
Βλάβη γαστρικού
βλεννογόνου (μέσω υπεραιμίας και παραγωγής ελευθέρων ριζών) -
Ισχαιμική νέκρωση εντέρου (σχετίζεται με σηπτικό
shock) - Μορφολογικές αλλοιώσεις στην
άνω παγκρεατοδωδεκαδακτυλικη αρτηρία
Επίδραση στο
νεφρικό σύστημα:
Μείωση νεφρικής ροής
αίματος - Μείωση σπειραματικής διήθησης - Ελάττωση ποσού ούρων,
αύξηση επαναρρόφησης Na+,
K+ - Συμμετοχή στη
νεφρική ανοσολογική βλάβη - Πρόκληση
ιστολογικών αλλοιώσεων - Εναπόθεση
ανοσοσυμπλεγμάτων στα σπειράματα
Επίδραση
στο σύστημα αναπαραγωγής:
Συμμετοχή στην κινητοποίηση του σπέρματος - Στην ωορρηξία - Στην
εμφύτευση ωαρίου - Στην υπέρταση της εγκυμοσύνης - Παίζει ρόλο
στην έναρξη και διατήρηση του τοκετού
Επίδραση
στην εγκεφαλική λειτουργία:
Καταστροφή νευρώνων - Συμμετοχή στην ανάπτυξη και στην
αναγέννηση των νευρώνων - Ενεργοποίηση του άξονα
"υποθάλαμος-υπόφυση-επινεφρίδια" και
έκκριση ορμονών - Αλλαγές φαινοτύπων στο κεντρικό νευρικό
σύστημα - Αύξηση διαπερατότητας εγκεφαλικών αγγείων - Συμμετοχή
στη σκλήρυνση κατά πλάκας
|
Μηχανισμός δράσης του PAF
Η εμπλοκή του
PAF
σε τόσες πολλές καταστάσεις και σε τόσα κύτταρα φαίνεται στο Σχήμα 5: Πολλά κύτταρα όταν διεγερθούν από διάφορους παράγοντες βιοσυνθέτουν
PAF. Ο
PAF
στη συνέχεια, ουσιαστικά, επιδρά στα ίδια κύτταρα αλλά και σε ιστούς ασκώντας
διάφορες δράσεις, μερικές από τις οποίες δευτερογενώς διεγείρουν εκ νέου τα
αρχικά κύτταρα για παραγωγή
PAF.
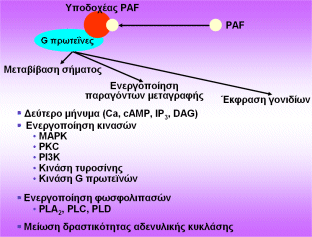
Το ευρύ φάσμα των βιολογικών δράσεων
του PAF μπορεί να ερμηνευθεί και από την πληθώρα
των δράσεων που προκαλούνται από τη μεταγωγή του σήματος, όταν ο
PAF
συνδεθεί με τον υποδοχέα του (Σχήμα 6). Δηλαδή, έχουμε μεταβίβαση σήματος,
ενεργοποίηση παραγόντων μεταγραφής και έκφραση γονιδίων.
Τα δεύτερα μηνύματα
αποτελούνται από τα γνωστά στοιχεία ή ενώσεις (ασβέστιο, κυκλική μονοφωσφορική
αδενοσίνη
cAMP, τριφωσφορική
ινοσιτόλη
IP3,
διακυλογλυκερόλες
DAG),
ενεργοποιούνται πολλές κινάσες, φωσφολιπάσες, αλλά και η
αδενυλική κυκλάση (AC).
Και όλα αυτά σε κάθε κύτταρο/ιστό/οργανισμό μπορεί να έχουν και διαφορετική
σημασία.
Θα πρέπει ακόμα να διευκρινιστεί ότι ο
PAF
ανήκει σε μια οικογένεια μορίων, στην
οποία ο PAF
είναι το δραστικότερο μέλος που είναι γνωστό έως σήμερα, υπόθεση που διατυπώθηκε
για πρώτη φορά στο 2nd
International Conference on Platelet-Activating
Factor and structurally related alkyl ether-lipids.
October 26-29, 1986, Tennessee, USA
από
τον Κ.Α. Δημόπουλο
κατά την ομιλία του με τίτλο
"Novel agents with PAF-like
activity and aspects on their physiological implication"
και η οποία υπόθεση ισχύει ακόμα.
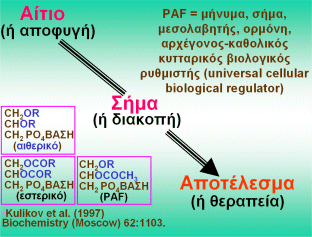
Επομένως, ο
PAF
είναι μήνυμα, σήμα,
μεσολαβητής, ορμόνη ή όπως αλλιώς έχει χαρακτηριστεί αρχέγονος-καθολικός
κυτταρικός βιολογικός ρυθμιστής (primordial
universal
cellular biological regulator)
(Σχήμα 7).
Μια ερμηνεία της πολυδιάστατης αυτής δράσης του
PAF
έχει δοθεί και από την ακόλουθη ενδιαφέρουσα θεωρία που διατυπώθηκε το 1997:
|

Σύμφωνα με τους
Kulikov και Muzya,
στις έντονες συνθήκες που επικρατούσαν στην αρχέγονη Γη, τα λιποειδή
με αιθερικούς δεσμούς, ως χημικώς σταθερότερα, μπορούσαν να "επιβιώσουν" περισσότερο από τα
αντίστοιχα λιποειδή με εστερικούς δεσμούς [Αναφ.
18]. |
Κατά τα πρώτα στάδια
εμφάνισης της ζωής στη Γη, οι
συνθήκες που επικρατούσαν ήταν σε σημαντικό βαθμό "εχθρικές" για τη ζωή
και τα διάφορα βιομόρια έπρεπε να
χαρακτηρίζονται μεγάλη χημική σταθερότητα. Φαίνεται λοιπόν ότι τα λιποειδή περιείχαν
σε μεγάλο βαθμό αιθερικούς και όχι
εστερικούς δεσμούς, οι οποίοι είναι χημικώς ασταθέστεροι σε σχέση με τους
πρώτους. Κατά την εξέλιξη των
συνθηκών προς ηπιότερες, όπως είναι σήμερα, οι αιθερικοί δεσμοί
σταδιακά αντικαταστάθηκαν από εστερικούς. Ωστόσο, κάποιες από αυτές τις
"αρχέγονες" λιποειδικές ενώσεις διατήρησαν μέχρι σήμερα τους αιθερικούς δεσμούς.
Είναι χαρακτηριστικό το γεγονός ότι οι γνωστές σήμερα λιποειδικές ενώσεις με αιθερικούς δεσμούς,
γενικά, παρουσιάζουν έντονη βιολογική
δραστικότητα. Μια από αυτές τις ενώσεις είναι και ο
PAF
[Αναφ.
18].
Αναστολείς της δράσης του
PAF. 'Ενα σήμα-μήνυμα
έχει σχεδόν πάντα τόσο ευεργετική όσο και επιβλαβή δράση ανάλογα με τις συνθήκες.
'Ετσι και η δράση του
PAF μπορεί να
είναι ευεργετική ή επιβλαβής για το
κύτταρο ή τον οργανισμό. Εδώ αναδεικνύεται και η μεγάλη σημασία των αναστολέων
του PAF.
Δηλαδή, αν δεν μπορεί να αποφευχθεί κάποια βλάβη ή δεν μπορεί να
θεραπευθεί το αποτέλεσμά της, μπορεί να ανασταλεί η εκδήλωση του ανεπιθύμητου
αποτελέσματος.
'Εχουν βρεθεί πολλοί αναστολείς του
PAF
φυσικής προέλευσης ή συνθετικοί.
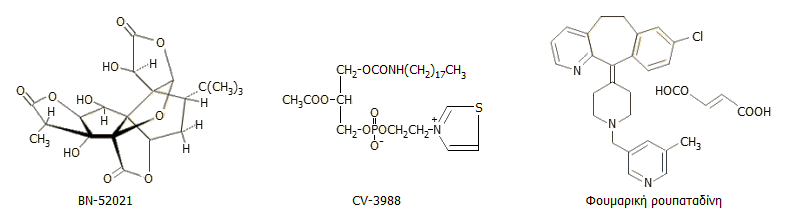
Στην πρώτη κατηγορία υπάγεται το
ΒΝ52021, ένα γκινγκολίδιο (συστατικό του φυτού
Ginkgo
biloba),
ο καλύτερος
(έως σήμερα)
φυσικός αναστολέας του
PAF και κάποια πολικά λιποειδή των Μεσογειακών
τροφίμων, στα οποία μάλιστα αποδίδεται και η προστατευτική δράση της Μεσογειακής δίαιτας
[Αναφ. 19] (βλ. στην
αναφορά σχετικό animation).
Στους συνθετικούς αναστολείς
υπάγεται το
CV-3988,
ένα δομικό ανάλογο του
PAF
[Αναφ. 20]
και η ρουπαταδίνη (rupatadine), το
πρώτο και μοναδικό φάρμακο-αναστολέας του
PAF,
που έχει κυκλοφορήσει. Αρχικά, η ρουπαταδίνη κυκλοφόρησε για την αλλεργική ρινίτιδα και κατόπιν για την ουρτικάρια (αλλεργικό κνησμό). Σημειώνεται ότι η ομάδα του Κ.Α. Δημόπουλου, με δημοσίευση το 1988, απέδωσε την αλλεργική ρινίτιδα στον
PAF
[Αναφ. 21]. Το 2003
δημοσιεύτηκε η σύνθεση της ρουπαταδίνης,
που είχε δράση αναστολέα του
PAF
αλλά και των H1 υποδοχέων της ισταμίνης και στη συνέχεια κυκλοφόρησε
ως φάρμακο για την αλλεργική ρινίτιδα με το όνομα Rupafin (Rupatadine
PAF
Inhibitor).
Τέλος, θα πρέπει να προστεθεί ότι οι αναστολείς του
PAF
είναι συνήθως και αναστολείς της βιοσύνθεσης του
PAF.
Συγκεκριμένα έχει αποδειχθεί ότι πολλοί αναστολείς του
PAF
αναστέλλουν κάποια ένζυμα-κλειδιά στις βιοσυνθετικές πορείες του
PAF
ή ενεργοποιούν το ένζυμο-κλειδί της αποδόμησης του
PAF.
|
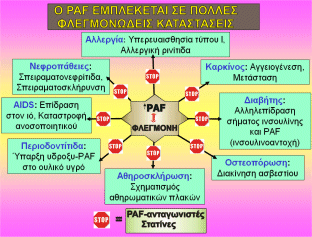
Σχήμα 8 |
Μέχρι σήμερα γνώσεις και
κενά.
Σήμερα η έρευνα
του PAF
έχει διευκρινίσει πάρα πολλά θέματα για τις δράσεις του, έχουν μελετηθεί ο
υποδοχέας του, ο μηχανισμός μεταγωγής του σήματός του
και τα ένζυμα και
η ρύθμιση του μεταβολισμού του, καθώς επίσης έχει βιοσυντεθεί με τη
σύγχρονη βιοτεχνολογία τόσο ο υποδοχέας του όσο και ένζυμα του μεταβολισμού του.
Πρόσφατα,
o
PAF εντοπίσθηκε στον
πυρήνα των κυττάρων, αλλά ο ρόλος του εκεί παραμένει
αδιευκρίνιστος. Αδιευκρίνιστα παραμένουν επίσης πολλά θέματα
σχετικά με την εμπλοκή του
PAF
στις διάφορες ασθένειες.
Η εμπλοκή και ο πρωταρχικός ρόλος του
PAF
σε πολλές ασθένειες γίνονται αντιληπτά από το γεγονός ότι ασθένειες που
σχετίζονται με την φλεγμονή σχετίζονται και με τον
PAF.
Συγκεκριμένα από τα μέχρι σήμερα γνωστά δεδομένα τα αυξημένα επίπεδα
PAF
προκαλούν φλεγμονή και στις φλεγμονώδεις καταστάσεις διαπιστώνονται αυξημένα
επίπεδα PAF.
Σε πολλές ασθένειες που σχετίζονται με τη φλεγμονή οι αναστολείς του
PAF
έχουν δείξει πειραματικά βελτίωση της κατάστασης. Αντίστοιχη δράση έχουν δείξει
και οι στατίνες
[Σημείωση 5] που και για αυτές όμως έχει αποδειχθεί ότι μία από τις
πλειοτροπικές δράσεις
[Σημείωση 6] τους είναι ότι αναστέλλουν τον
PAF
(Σχήμα 8).
Κατά συνέπεια, οι αναστολείς του
PAF,
είτε με τη μορφή φαρμάκων είτε με την πρόσληψη από την τροφή, πιθανόν να έχουν
σημαντικό ρόλο στην αντιμετώπιση αλλά και στην πρόληψη των ασθενειών.


Σημείωση 5: Οι
στατίνες (ή αναστολείς της αναγωγάσης HMG-CoA) είναι μια τάξη
φαρμάκων που χαμηλώνουν τα επίπεδα χοληστερόλης σε άτομα που πάσχουν ή
κινδυνεύουν να πάθουν καρδιαγγειακές νόσους.
Σημείωση 6:
Ως πλειοτροπικές δράσεις των
στατινών χαρακτηρίζονται οι ιδιότητές τους που δεν αφορούν τη μείωση των
επιπέδων χοληστερόλης στο αίμα. Σήμερα έχουν βρεθεί πολλές τέτοιες ιδιότητες και
συνεχώς βρίσκονται και άλλες, με αποτέλεσμα να επανεξετάζεται το κατά πόσο τα
ευεργετικά αποτελέσματα των στατινών οφείλονται στη μείωση των επιπέδων της χοληστερόλης.
Ακόμη, επανεξετάζεται και η σημασία των επιπέδων της
χοληστερόλης.
|
Μικροφωτογραφία θρόμβου
αίματος |
Συσσώρευση αιμοπεταλίων
[Αναφ. 1β]
Σημαντικό ρόλο στη δημιουργία του θρόμβου παίζουν
τα αιμοπετάλια τα οποία είναι θραύσματα των μεγακαρυοκυττάρων.
Μορφολογικά τα αιμοπετάλια είναι κύτταρα χωρίς πυρήνα, τα οποία περιέχουν
εκτεταμένο δίκτυο από μικροσωληνίσκους και από το σύστημα ακτίνης/μυοσίνης. 'Οταν
δεν είναι ενεργοποιημένα, η κυτταροπλασματική τους μεμβράνη έχει πολλές
πτυχώσεις προς το εσωτερικό του κυττάρου. Κατά την ενεργοποίησή τους, η
κυτταροπλασματική τους μεμβράνη εκτείνεται προς το εξωτερικό μέρος παρέχοντας
εύκολη πρόσβαση στους υποδοχείς και στα φωσφολιποειδή, που είναι απαραίτητα για
τη διαδικασία της πήξης.
Τα αιμοπετάλια περιέχουν διάφορα κοκκία τα οποία
περιέχουν α) ασβέστιο, ADP και σεροτονίνη, β) ανταγωνιστές της ηπαρίνης, PDGF,
παράγοντα von Willebrand (vWF), ινωδογόνο και β-θρομβοσφαιρίνη και γ) υδρολυτικά
ένζυμα. Ο vWF παράγεται από τα ενδοθηλιακά κύτταρα, τα μεγακαρυοκύτταρα και
επιπλέον βρίσκεται συνδεδεμένος με τον παράγοντα πήξης VIII.
Σημαντικό ρόλο στη δημιουργία του θρόμβου παίζουν
τα αιμοπετάλια τα οποία είναι θραύσματα των μεγακαρυοκυττάρων. Μορφολογικά τα
αιμοπετάλια είναι κύτταρα χωρίς πυρήνα, τα οποία περιέχουν εκτεταμένο δίκτυο από
μικροσωληνίσκους και από το σύστημα ακτίνης/μυοσίνης. 'Οταν δεν είναι
ενεργοποιημένα, η κυτταροπλασματική τους μεμβράνη έχει πολλές πτυχώσεις προς το
εσωτερικό του κυττάρου. Κατά την ενεργοποίησή τους, η κυτταροπλασματική τους
μεμβράνη εκτείνεται προς το εξωτερικό μέρος παρέχοντας εύκολη πρόσβαση στους
υποδοχείς και στα φωσφολιποειδή, που είναι απαραίτητα για τη διαδικασία της
πήξης.
Τα αιμοπετάλια περιέχουν διάφορα κοκκία τα οποία
περιέχουν α) ασβέστιο, ADP και σεροτονίνη, β) ανταγωνιστές της ηπαρίνης, PDGF,
παράγοντα von Willebrand (vWF), ινωδογόνο και β-θρομβοσφαιρίνη και γ) υδρολυτικά
ένζυμα. Ο vWF παράγεται από τα ενδοθηλιακά κύτταρα, τα μεγακαρυοκύτταρα και
επιπλέον βρίσκεται συνδεδεμένος με τον παράγοντα πήξης VIII.
|
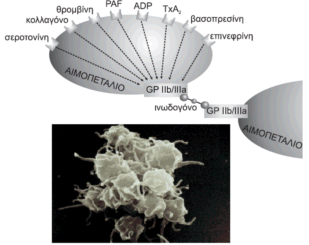
Σχήμα 9 |
Η ενεργοποίηση των αιμοπεταλιών περιλαμβάνει την
προσκόλλησή τους στον υποενδοθηλιακό χώρο. Σε φυσιολογικές καταστάσεις τα
αιμοπετάλια δεν προσκολλούνται στο ενδοθήλιο, αλλά μόνο σε καταστάσεις που έχει
υποστεί βλάβη το αγγειακό τοίχωμα και εκτίθενται τα συστατικά του
υποενδοθηλιακού χώρου (όπως το κολλαγόνο και ο vWF) στην κυκλοφορία του αίματος.
Στη μεμβράνη των αιμοπεταλίων βρίσκονται
γλυκοπρωτεΐνες (ιντεγκρίνες) οι οποίες δεσμεύονται με το κολλαγόνο και τον vWF
οδηγώντας σε προσκόλλησή τους στο υποενδοθήλιο. Η συνάθροιση με αυτόν τον τρόπο
περισσότερων αιμοπεταλίων στον υποενδοθηλιακό χώρο σχηματίζει μια στιβάδα στην
περιοχή της βλάβης. Η δέσμευση των αιμοπεταλίων στο υποενδοθήλιο προκαλεί την
ενεργοποίησή τους, η οποία περιλαμβάνει την αύξηση του ενδοκυτταρικού ασβεστίου
που προκαλεί την αλλαγή του σχήματός τους (από δισκοειδές σε σφαιρικό με
ψευδοπόδια), μεταβολές του μεταβολισμού τους και αποκοκκίωση. Η αλλαγή αυτή του
σχήματος οδηγεί σε αύξηση της ενεργής -για αλληλεπιδράσεις- επιφάνειας των
κυττάρων. Σε αυτή τη φάση ενεργοποιούνται και άλλες γλυκοπρωτεΐνες στην
επιφάνεια των αιμοπεταλίων και ακολουθεί η φάση της συσσώρευσης των
αιμοπεταλίων, η οποία περιλαμβάνει τη μεταξύ τους συγκόλληση.
Οι παράγοντες που προκαλούν τη συσσώρευση των
αιμοπεταλίων ονομάζονται αγωνιστές και μπορεί να παράγονται από τα ίδια τα
αιμοπετάλια ή άλλα κύτταρα που εμπλέκονται στη διαδικασία. Μεταξύ αυτών είναι το
ADP, η θρομβίνη, το κολλαγόνο και ο PAF (Σχήμα 9).
Η απελευθέρωση και η σύνθεση διαφόρων μεσολαβητών
από τα ενεργοποιημένα αιμοπετάλια συμπεριλαμβανομένης και θρομβοξάνης Α2,
προκαλεί τη συστολή των αγγείων και τη μείωση της ροής του αίματος στην περιοχή
της βλάβης. Είναι σημαντικό επίσης να αναφερθεί ότι η συσσώρευση των
αιμοπεταλίων που πραγματοποιείται στην περιοχή της βλάβης δημιουργεί ένα
αιμοπεταλιακό κάλυμμα του οποίου η επέκταση σε φυσιολογικές περιοχές
αναστέλλεται.
Μεταγωγή του σήματος από τον υποδοχέα του PAF
[Αναφ. 1β]
Ο PAF εκδηλώνει τη δράση του, μέσω
επταδιαμεμβρανικών υποδοχέων που συνδέονται με Gq πρωτεΐνες. 'Ετσι
ενεργοποιείται το ένζυμο της φωσφολιπάσης C (PLC) προς παραγωγή τριφωσφορική
ινοσιτόλης (IP3), διακυλογλυκερόλης (1,2 DAG) και τροποποιούνται τα επίπεδα του
ενδοκυτταρικού ασβεστίου. Η σύνδεση του PAF με τον υποδοχέα του οδηγεί επίσης σε
μεταγωγή σήματος μέσω ενεργοποίησης καταρρακτών MAP κινασών, οι οποίες είναι σε
θέση να φωσφορυλιώσουν και να ενεργοποιήσουν τη φωσφολιπάση Α2 (PLΑ2) στην
κυτταροπλασματική μεμβράνη. Το γεγονός αυτό μεταξύ άλλων οδηγεί στην
απελευθέρωση αραχιδονικού οξέος και τελικά στη βιοσύνθεση των εικοσανοειδών (θρομβοξάνια,
λευκοτριένια, προσταγλανδίνες).
 Ρόλος
του PAF στην αναπαραγωγή
Ρόλος
του PAF στην αναπαραγωγή
Σημαντικότατος είναι και ο ρόλος του PAF σε όλα τα
στάδια της αναπαραγωγής του ανθρώπου. Συγκεκριμένα στην ωορρηξία, στη
γονιμοποίηση, στην ανάπτυξη του εμβρύου και στον τοκετό. Χαρακτηρίζεται ως
εμβρυοτροφίνη (embryotrophin) και είναι ο πρώτος τροφικός παράγοντας, που βιοσυντίθεται από το έμβρυο τις πρώτες ώρες στα αρχικά στάδια του εμβρύου και
ρυθμίζει τις διάφορες διεργασίες της ανάπτυξής του, ενώ παράγεται συγχρόνως και
από το αναπαραγωγικό σύστημα της γυναίκας [Αναφ. 22α].
PAF έχει βρεθεί και στο σπέρμα και φαίνεται πως παίζει σημαντικό ρόλο στην κινητικότητά του και
επομένως στη
διαδικασία της γονιμοποίησης [Αναφ. 22β].
Σήμερα ο PAF χρησιμοποιείται στην τεχνητή γονιμοποίηση
-και στην Ελλάδα- τόσο στη βελτίωση της κινητικότητας του σπέρματος όσο και στα
άλλα στάδια αυτής.
Μια νέα προσέγγιση στον καρκίνο
Ο
PAF αποτελεί έναν σημαντικό μεσολαβητή και σε διάφορές καρκινικές καταστάσεις. Η
ανάπτυξη των καρκινικών όγκων και η μεταστατική τους ικανότητα εξαρτάται από τον
σχηματισμό νέων αγγείων που συνδέονται τόσο με τον όγκο όσο και με το
κυκλοφορικό σύστημα με μια διαδικασία γνωστή και ως νεοαγγειογένεση.
Διάφοροι μεσολαβητές όπως ο PAF, κυτταροκίνες, αυξητικοί παράγοντες, κ.α.
συμμετέχουν στην όλη διαδικασία. Η παρουσία του PAF στο μικροκαρκινικό
περιβάλλον αποτελεί σημαντικό κομβικό σημείο αυτών των σηματοδοτικών
αλληλουχιών, καθώς η δράση του τόσο στα καρκινικά κύτταρα όσο και στα
παρακείμενα αγγειακά ενδοθηλιακά κύτταρα προάγει και επάγει καθοριστική ενίσχυση
του αρχικού καρκινικού μεταστατικού σήματος.
Η
προσπάθεια αναστολής του μεταστατικού σήματος έχει μετατοπιστεί πλέον στην
αναστολή των δράσεων κομβικών μεσολαβητών όπως ο PAF ή/και στη μείωση των
επιπέδων τους (μέσω αναστολής της βιοσύνθεση τους ή/και επάγοντας την
αποδόμηση τους). 'Ενα διαιτητικό μοντέλο - όπως αυτό της Μεσογειακής
δίαιτας - πλούσιο σε αντιοξειδωτικά και σε αναστολείς του PAF, αλλά και των
βιοσυνθετικών του ενζύμων, φαίνεται ότι προσφέρει μια μη τοξική προληπτική και
θεραπευτική προσέγγιση έναντι της μετάστασης και της ανάπτυξης του καρκινικού
όγκου [Αναφ. 23].
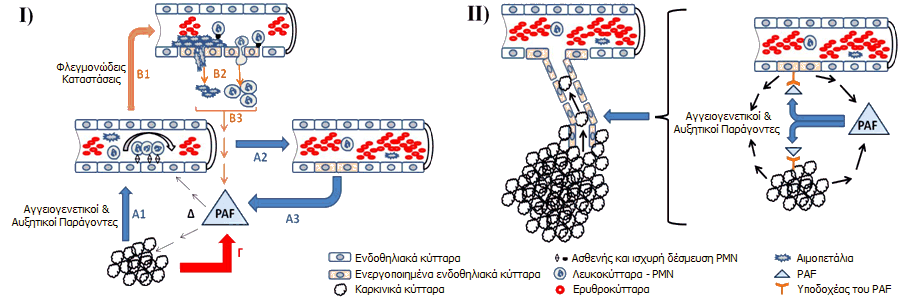
Μηχανισμός σύνθεσης
(Ι) και συμμετοχής (ΙΙ) του PAF στην νεοαγγειογένεση και μετάσταση
των καρκινικών κυττάρων
Ο μηχανισμός σύνθεσης
και συμμετοχής του PAF στην νεοαγγειογένεση και στη μετάσταση
των καρκινικών κυττάρων, συνοπτικά παρουσιάζεται στο επάνω σχήμα και
έχει ως εξής:
Ι) Σύνθεση PAF στο
μικροκαρκινικό περιβάλλον: (1)Τα καρκινικά κύτταρα μέσω της έκκρισης αγγειογενετικών παραγόντων
ενεργοποιούν τα ενδοθηλιακά κύτταρα προς παραγωγή PAF (Πορεία
A1-A3). (2) Ο PAF μπορεί να συντεθεί από διηθούντα φλεγμονώδη κύτταρα
(λευκοκύτταρα και αιμοπετάλια) σε φλεγμονώδεις καταστάσεις (Πορεία
Β1-Β3). (3) Τέλος, ο PAF μπορεί να συντεθεί από τα ίδια τα καρκινικά κύτταρα
(Πορεία Γ).
ΙΙ) Επιδράσεις του PAF:
(1) Ο παραγόμενος PAF καθώς
συνδέεται στον υποδοχέα του, τόσο στα ενδοθηλιακά όσο και στα
καρκινικά κύτταρα, επάγει με καταρράκτη δεύτερων μηνυμάτων την
περαιτέρω ενεργοποίηση αυτών των κυττάρων για επανασύνθεση τόσο του
PAF όσο και αγγειογενετικών και αυξητικών παραγόντων ενισχύοντας
έτσι το αρχικό σήμα. (2) Στα καρκινικά κύτταρα ενεργοποιούνται μηχανισμοί μιτωτικού
πολλαπλασιασμού, κινητικότητας, έκφρασης μορίων συγκόλλησης,
διεισδυτικότητας, μετανάστευσης (μετάστασης).
(3) Στα ενδοθηλιακά κύτταρα ενεργοποιούνται μηχανισμοί αποδόμησης
της εξωκυττάριας ουσίας, μιτωτικού πολλαπλασιασμού, κινητικότητας,
έκφρασης μορίων συγκόλλησης, μετανάστευσης και αναδιάταξης προς
σχηματισμό νεόπλαστων μικρών νέων αγγείων.
(4) Τελικό αποτέλεσμα είναι η μεταφορά θρεπτικών ουσιών από το αίμα
στον καρκινικό όγκο αλλά και η μετάσταση των καρκινικών κυττάρων
μέσω των νεοσχηματιζόμενων αγγειωμάτων και του αίματος σε άλλους
ιστούς.
Βιβλιογραφία - Πηγές από το
Διαδίκτυο
1.
(α) Δημόπουλος ΚΑ: Παρουσίαση
PAF (διαλέξεις Τμήματος Χημείας) (αρχείο
PDF, 7,1 MB). (β) Δημόπουλος ΚΑ, Αντωνοπούλου Σ:
"Βασική
Βιοχημεία", 2η έκδοση, 2009. (γ) Wikpedia: "Platelet-activating
factor".
(δ) Pinckard RN, McManus LM,
Demopoulos CA, Halonen M, Clark PO, Shaw JO, Kniker WT, Hanahan DJ:
"Molecular pathobiology of acetyl glyceryl
ether phosphorylcholine: evidence for the structural and functional identity
with platelet-activating factor",
J Reticuloendothel Soc.,
28(Suppl):95s-103s, 1980.
2. Barbaro JF,
Zvaifler NJ: "Antigen induced histamine release from platelets of rabbits
producing homologous PCA antibody",
Proceedings of the
Society for Experimental Biology and Medicine, 122(4):1245-1247,
1966.
3.
Henson PM:
"Release of vasoactive amines from rabbit platelets
induced by sensitized mononuclear leukocytes and antigen",
Journal of Experimental Medicine, 131(2):287-306,
1970 (PubMed).
4. (α)
Siraganian RP, Osler AG: "Destruction of rabbit platelets in
the allergic response of sensitized leukocytes. I. Demonstration of a fluid
phase intermediate. Journal of Immunology, 106(5), 1244-1251, 1971 (Abstract).
(β) Siraganian RP, Osler AG: "Destruction of rabbit platelets
in the allergic response of sensitized leukocytes. II. Evidence for basophil
involvement", Journal of Immunology, 106(5):1252-1259, 1971
(Abstract).
5.
Benveniste J,
Henson PM, Cochrane CG:
"Leukocyte-dependent
histamine release from rabbit platelets. The role of IgE, basophils, and a
platelet-activating factor",
Journal of Experimental Medicine, 136(6):1356-1377,
1972 (PubMed,
πλήρες άρθρο:
αρχείο PDF, 1,5 MB).
6. (α) Wikipedia: "Allergy".
(β) Henson PM,
Pinckard RN: "Basophil-derived platelet-activating factor (PAF) as an in vivo
mediator of acute allergic reactions: Demonstration of specific desensitization
of platelets to PAF during IgE-induced anaphylaxis in the rabbit", Journal of
Immunology, 119(6):2179-2184, 1977 (Abstract).
(γ) Henson PM, Pinckard RN:
"Platelet activating factor (PAF). A possible direct mediator of anaphylaxis in
the rabbit and a trigger for the vascular deposition of circulating immune
complexes", Monographs in Allergy, 12:13-26, 1977 (PubMed).
7. (α)
Wikipedia: "Arthus
reaction". (β)
Pinckard RN, Farr RS, Hanahan DJ:
"Physicochemical
and functional identity of rabbit platelet-activating factor (PAF) released in
vivo during IgE anaphylaxis with PAF released in vitro from IgE sensitized
basophils",
Journal of Immunology, 123(4):1847-1857,
1979 (Abstract).
8. Demopoulos
CA,
Pinckard RN, Hanahan DJ:
"Platelet-activating
factor. Evidence for 1-O-alkyl-2-acetyl-sn-glyceryl-3-phosphorylcholine as the
active component (a new class of lipid chemical mediators)",
Journal of Biological Chemistry, 254(19), 9355-9358,
1979 (αρχείο
PDF, 976 KB).
9. (α) ITP Aware: "What
is a Platelet?". (β) Wikipedia: "Platelet".
10. Hanahan DJ, Demopoulos
CA, Liehr J, Pinckard RN: "Identification of platelet activating factor isolated
from rabbit basophils as acetyl glyceryl ether phosphorylcholine", Journal
of Biological Chemistry, 255(12):5514-5516, 1980 (αρχείο
PDF, 424 KB).
11.
Blank ML, Snyder F, Byers LW,
Muirhead ΕΕ:
"Antihypertensive activity of an alkyl ether analog of
phosphatidylcholine", Biochemical and Biophysical
Research Communications, 90(4):1194-1200,
1979 (Abstract).
12. Cusack
NJ: "Platelet-activating
factor", Nature, 285(5762):193,
1980.
13. Demopoulos CA: "State
of lipid research in Greece", European Journal of Lipid Science and Technology,
102(11):Editorial, 2000 (αρχείο
PDF, 443 KB).
14.
(α) McManus LM, Hanahan DJ, Demopoulos CA, Pinckard RN:
"Pathobiology of the intravenous infusion of acetyl
glyceryl ether phosphorylcholine (AGEPC), a synthetic platelet-activating factor
(PAF), in the rabbit", Journal of Immunology, 124(6):2919-2924,
1980.
(β) Halonen M, Palmer JD, Lohman IC, McManus LM,
Pinckard RN: "Respiratory and circulatory alterations induced by acetyl glyeryl
ether phosphorylcholine (AGEPC), a mediator of IgE anaphylaxis in the rabbit",
Am Rev Resp Dis 122:915924,
1980 (PubMed).
(γ) Pinckard RN, McManus
LM, Orourke RA, Crawford MH, Hanahan DJ: "Intravascular and cardiovascular
effects of acetyl glyceryl ether phosphorylcholine (AGEPC) infusion in the
baboon", Clinical Research, 28(2):A358-A358, 1980. (δ) Halonen M, Palmer JD, Lohman IC, McManus LM, Pinckard RN:
"Differential effects of platelet depletion on the physiologic alterations of
IgE anaphylaxis, and acetyl glyceryl ether phosphorylcholine infusion in the
rabbit", Am er. Rev. resp. Dis., 124:416-421, 1981 (PubMed).
15.
Pinckard RN, Kniker WT, Lee L, Hanahan DJ, McManus LM:
"Vasoactive Effects of 1-Ο-Alkyl-2-Acetyl-sn-Glyceryl-3-Phosphorycholine
(Acgepc) in Human-Skin", Journal of Allergy and Clinical Immunology,
65(3):196-196, 1980.
16. Vadas P, Gold M,
Perelman B, Liss GM, Lack G, Blyth T, Simons FER, Simons KJ, Cass D, Yeung J: "Platelet-Activating
Factor, PAF acetylhydrolase, and severe anaphylaxis", New England Journal of
Medicine, 358(1):28-35, 2008.
17. Shibamoto
T, Liu W, Cui S, Zhang W, Takano H, Kurata Y: "PAF, rather than histamine,
participates in mouse anaphylactic hypotension", Pharmacology, 82(2):114-120,
2008 (Abstract).
18.
Kulikov VI,
Muzya GI: "Ether lipids and platelet-activating factor: evolution and cellular
function", Biochemistry (Moscow), 62(10):1103-1108, 1997 (PubMed).
19. Δημόπουλος ΚΑ, Καραντώνης ΧΚ,
Αντωνοπούλου Σ: "Η
θεωρία της αθηροσκλήρωσης με εμπλοκή του PAF" (Ιστοσελίδες του Τμήματος
Χημείας, ΕΚΠΑ).
20. Arnout J, van Hecken A, De Lepeleire I,
Miyamoto Y, Holmes I, De Schepper P, Vermylen J: "Effectiveness and tolerability
of CV-3988, a selective PAF antagonist, after intravenous administration to man",
Br J Clin Pharmacol.,
25(4):445-451, 1988. (αρχείο
PDF, 932 KB).
21.
(α) Labrakis-Lazana K, Lazanas M, Koussissis
S, Tournis S, Demopoulos C: "PAF of biological fluids in disease:
blood levels in allergic rhinitis", Haematologica, 73:379-382, 1988.
(β)
Albert DH, Malo PE, Tapang P, Shaughnessy TK, Morgan
DW, Wegner CD, Curtin ML, Sheppard GS, Xu L,
Davidsen SK, Summers JB, Carter GW: "The
Role of Platelet-Activating Factor (PAF) and the Efficacy of ABT-491, a Highly
Potent and Selective PAF Antagonist, in Experimental Allergic Rhinitis",
Pharmacology and Experimental Therapeutics,
284(1):83-88, 1998.
22. (α) O'Neill C: "The
role of paf in embryo physiology",
Human Reproduction Update, 11(3):215-228, 2005.
(β) Roudebush WE, Massey JB, Elsner CW,
Shapiro DB, Mitchell-Leef D, Kort HI: "The significance of platelet-activating
factor and fertility in the male primate: a review",
J Med Primatol., 34(1):20-24, 2005 (PubMed).
23.
Tsoupras AB,
Iatrou C, Frangia C,
Demopoulos: "The Implication of Platelet Activating
Factor in cancer growth and
metastasis: Potent beneficial
role of PAF-inhibitors and
antioxidants",
Infectious Disorders - Drug Targets,
9:390-399, 2009 (Abstract).
|
Αποποίηση
ευθυνών: Έχει καταβληθεί κάθε προσπάθεια για να εξασφαλισθεί η
ορθότητα των πληροφοριών που περιλαμβάνονται σε αυτή τη σελίδα, ωστόσο ο
έχων την επιμέλεια της σελίδας αυτής και το Τμήμα Χημείας δεν αναλαμβάνουν
τη νομική ευθύνη για τυχόν σφάλματα, παραλείψεις ή ανακριβείς πληροφορίες.
Επιπλέον, το Τμήμα Χημείας δεν εγγυάται την ορθότητα των αναφερόμενων σε
εξωτερικές ιστοσελίδες, ούτε η αναφορά μέσω συνδέσμων (links) στις
ιστοσελίδες αυτές, υποδηλώνει ότι το Τμήμα Χημείας επικυρώνει ή καθ'
οιονδήποτε τρόπο αποδέχεται το περιεχόμενό
τους. |

 Συνοπτική
παρουσίαση του
Συνοπτική
παρουσίαση του  Ο
παράγοντας ενεργοποίησης αιμοπεταλίων
(
Ο
παράγοντας ενεργοποίησης αιμοπεταλίων
(





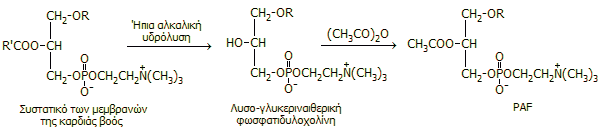

 Σημείωση
2:
Το πρόθημα λυσο- στα γλυκερίδια, δηλώνει την παρουσία ελεύθερου
γλυκερινικού υδροξυλίου.
Σημείωση
2:
Το πρόθημα λυσο- στα γλυκερίδια, δηλώνει την παρουσία ελεύθερου
γλυκερινικού υδροξυλίου.

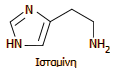 Δυο
λόγια για την ισταμίνη
Δυο
λόγια για την ισταμίνη






 Ρόλος
του PAF στην αναπαραγωγή
Ρόλος
του PAF στην αναπαραγωγή