Τι είναι η L-DOPA ή λεβοντόπα [Αναφ. 1]
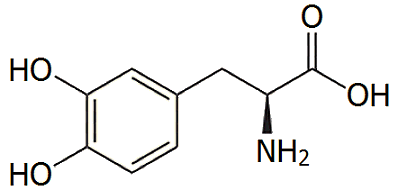
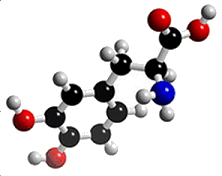 Η L-DOPA (L-3,4-διυδροξυφαινυλαλανίνη)
ή λεβοντόπα (σύμφωνα με την Ελληνική Φαρμακοποιία) είναι μια φαρμακευτική ουσία με έντονη βιοχημική
δράση, η οποία παράγεται φυσιολογικά στον άνθρωπο κατά τον μεταβολισμό του αμινοξέος L-τυροσίνη.
Από χημική άποψη πρόκειται για ένα α-αμινοξύ, το οποίο όμως δεν συναντάται
στις πρωτεΐνες. Η L-DOPA συναντάται σε ορισμένα φυτά, όπως στον κύαμο (Vicia faba) από τους
καρπούς του οποίου απομονώθηκε για πρώτη φορά.
Η L-DOPA (L-3,4-διυδροξυφαινυλαλανίνη)
ή λεβοντόπα (σύμφωνα με την Ελληνική Φαρμακοποιία) είναι μια φαρμακευτική ουσία με έντονη βιοχημική
δράση, η οποία παράγεται φυσιολογικά στον άνθρωπο κατά τον μεταβολισμό του αμινοξέος L-τυροσίνη.
Από χημική άποψη πρόκειται για ένα α-αμινοξύ, το οποίο όμως δεν συναντάται
στις πρωτεΐνες. Η L-DOPA συναντάται σε ορισμένα φυτά, όπως στον κύαμο (Vicia faba) από τους
καρπούς του οποίου απομονώθηκε για πρώτη φορά.
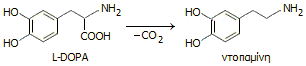 H L-DOPA είναι η
κυριότερη φαρμακευτική ουσία για την αντιμετώπιση των
συμπτωμάτων της
νόσου του Parkinson,
μιας εκφυλιστικής κατάστασης του κεντρικού νευρικού συστήματος, η οποία είναι γνωστή και ως τρομώδης παράλυση (shaking pulsy). Μέχρι σήμερα
δεν έχει βρεθεί άλλη αποτελεσματικότερη φαρμακευτική ουσία που θα μπορούσε
να αντικαταστήσει την L-DOPA για τον σκοπό αυτό.
H L-DOPA είναι η
κυριότερη φαρμακευτική ουσία για την αντιμετώπιση των
συμπτωμάτων της
νόσου του Parkinson,
μιας εκφυλιστικής κατάστασης του κεντρικού νευρικού συστήματος, η οποία είναι γνωστή και ως τρομώδης παράλυση (shaking pulsy). Μέχρι σήμερα
δεν έχει βρεθεί άλλη αποτελεσματικότερη φαρμακευτική ουσία που θα μπορούσε
να αντικαταστήσει την L-DOPA για τον σκοπό αυτό.
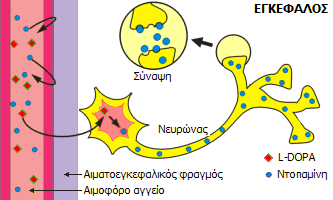
Τα νευρικά κύτταρα του εγκεφάλου χρησιμοποιούν τη χορηγούμενη L-DOPA για να συνθέσουν βιοχημικά την ουσία ντοπαμίνη (3-υδροξυτυραμίνη), έναν από τους σημαντικότερους νευροδιαβιβαστές (neurotransmitter), δηλ. τις ουσίες μέσω των οποίων επικοινωνούν οι νευρώνες (νευρικά κύτταρα). 'Ετσι, η L-DOPA παρέχει την απαραίτητη ντοπαμίνη στον εγκέφαλο, όπου δεν μπορεί να παραχθεί λόγω της νόσου του Parkinson. Η ντοπαμίνη δεν μπορεί να χορηγηθεί απ' ευθείας ως φάρμακο δια του στόματος, επειδή δεν μπορεί να διαπεράσει τον αιματοεγκεφαλικό φραγμό (blood-brain barrier, BBB) και να εισέλθει στον εγκέφαλο.
Ιστορία της ανακάλυψης της L-DOPA [Αναφ. 2]
Το 1911, ο διάσημος Πολωνός βιοχημικός Casimir Funk (1884-1967), διάσημος για τις μελέτες του στις βιταμίνες (καθιέρωσε τον όρο "βιταμίνη", βλ. Χημική ένωση του μήνα: L-ασκορβικό οξύ), συνέθεσε τη ρακεμική D,L-3,4-διυδροξυφαινυλαλανίνη (D,L-DOPA) στα πλαίσια μιας μελέτης του πάνω στη βιοσύνθεση της αδρεναλίνης, πιστεύοντας (ορθά) ότι είναι μια από τις πρόδρομες ενώσεις της. Επιπλέον, ήθελε να διαπιστώσει αν η ένωση αυτή, ως α-αμινοξύ, βρίσκεται σε πρωτεΐνες.
Το 1913, ο Ελβετός βιοχημικός Marcus Guggenheim (1885-1970) απομόνωσε την L-DOPA από τους καρπούς-σπέρματα του κυάμου (Vicia faba), τα γνωστά κουκιά, τα οποία είναι πλουσιότατα σε πρωτεΐνες (20-25%) και περιέχουν L-DOPA (ανώριμοι, πράσινοι καρποί) μέχρι και 0,6%. Πρέπει να σημειωθεί ότι η L-DOPA βρίσκεται σε ιστούς πολλών φυτικών οργανισμών και συχνά σε πολύ μεγαλύτερες περιεκτικότητες. Χαρακτηριστική περίπτωση αποτελεί το τροπικό φυτό Mucuna urens, στα σπέρματα του οποίου η περιεκτικότητα σε L-DOPA φθάνει το 6-8%. Σε αρχαιότατα Ινδουιστικά κείμενα περιγράφεται η νόσος Kampa vata με συμπτώματα επακριβώς ίδια με εκείνα της νόσου του Parkinson. Για τη συμπτωματική θεραπεία της νόσου αυτής οι αρχαίοι Ινδοί χορηγούσαν σπέρματα αυτού του φυτού (Αγιουρβεδική ιατρική). [Συμπτωματική θεραπεία (symptomatic treatment) νόσου: Θεραπεία που αποβλέπει στην ανακούφιση του ασθενούς από τα συμπτώματα μιας νόσου και όχι στη θεραπεία της ίδιας της νόσου]
Λόγω της χημικής δομής της L-DOPA, ο Guggenheim υποπτεύθηκε ότι η ένωση αυτή αποτελεί πρόδρομη ένωση της αδρεναλίνης (βλ. Χημική ένωση του μήνα: Αδρεναλίνη) και επομένως θα έπρεπε να είναι μια βιολογικώς ενεργή ουσία. Για να δοκιμάσει την υπόθεσή του δεν δίστασε να χορηγήσει στον εαυτό του 2,5 g της νέας ένωσης, όμως το μόνο που διαπίστωσε ήταν μια έντονη παροδική αδιαθεσία και εμετική δράση. Ο Guggenheim συνέχισε τα πειράματά του με κουνέλια και κατέληξε στο συμπέρασμα ότι η ουσία δεν παρουσίαζε κάποια αξιόλογη βιολογική δράση. Η γνώμη αυτή επεκράτησε στην επιστημονική κοινότητα για περίπου 15 χρόνια.
 |
 |
 |
 |
|
Από αριστερά προς τα δεξιά: (1) ο Ελβετός βιοχημικός Marcus Guggenheim (1885-1970) (αριστερά), Διευθυντής Φαρμακολογίας, της Φαρμακευτικής Βιομηχανίας Roche στη Γερμανική πόλη Grenzach-Wyhlen [πηγή]. (2-3) Κύαμος (Vicia faba), οι λοβοί και τα σπέρματά του (κουκιά) από τα οποία ο Guggenheim απομόνωσε για πρώτη φορά την L-DOPA το 1913. (4) Λοβοί του τροπικού φυτού Mucuna pruriens που ανήκει στην οικογένεια των κυαμοειδών (Fabaceae). Τα σπέρματα του φυτού αυτού είναι ιδιαιτέρως πλούσια σε L-DOPA (6-8%) και χρησιμοποιήθηκαν από τους αρχαίους Ινδούς για τη θεραπεία των συμπτωμάτων της νόσου Kampa vata, η οποία από τις περιγραφές των συμπτωμάτων της φαίνεται πως ήταν η νόσος του Parkinson [πηγή]. |
|||
Το 1927, διάφορες βιοχημικές μελέτες με L-DOPA έδειξαν ότι η ουσία αυτή μείωνε δραστικά την πίεση του αίματος σε κουνέλια. Το 1938, ο Peter Holz (1902-1970) πειραματιζόμενος με την L-DOPA διαπίστωσε ότι σε ιστούς θηλαστικών η ένωση αποκαρβοξυλιώνεται παρέχοντας ντοπαμίνη. Kατά τη δεκαετία του 1940, διεξήχθησαν πειράματα σε γάτες και ανθρώπους, τα οποία επιβεβαίωσαν ότι η χορήγηση L-DOPA γενικά αυξάνει τα επίπεδα ντοπαμίνης στους διάφορους ιστούς του σώματος.
Κατά τη δεκαετία του 1950, ιατρικές έρευνες έδειξαν τη φυσιολογική παρουσία L-DOPA σε πολλούς ιστούς και κυρίως στον εγκέφαλο. Οι έρευνες συνεχίστηκαν με στόχο να αποδείξουν ότι η ουσία αυτή αποτελεί πρόδρομη ένωση της αδρεναλίνης και άλλων κατεχολαμινών (παραγώγων του 1,2-διυδροξυβενζολίου, μιας φαινολικής ένωσης γνωστής με την εμπειρική ονομασία "κατεχόλη"). Η ντοπαμίνη είναι ένας από τους κυριότερους νευροδιαβιβαστές, των ουσιών μέσω των οποίων επικοινωνούν μεταξύ τους τα νευρικά κύτταρα (νευρώνες) στις περιοχές των συνάψεών τους. Μέχρι σήμερα έχουν ανακαλυφθεί περίπου 50 νευροδιαβιβαστές. Οι συντακτικοί τύποι της μητρικής ένωσης και των κυριότερων κατεχολαμινών δίνονται παρακάτω.
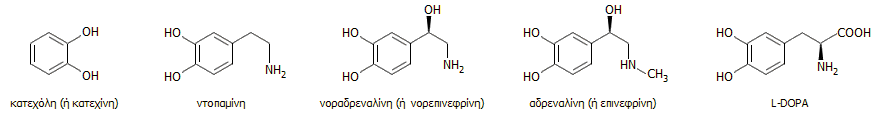
Πρώτες ενδείξεις της φαρμακευτικής δράσης της L-DOPA [Αναφ. 3]
 |
 |
 |
|
Οι βραβευθέντες με το βραβείο Nobel του 2000 ιατροί για τις μελέτες τους σε σχέση με τη μεταγωγή νευρικών σημάτων. Από αριστερά προς τα δεξιά: Arvid Carlsson (Uppsala, Σουηδία, 1923), Eric Kandel (Γερμανία, 1929), Paul Greengard (Νέα Υόρκη, 1925). |
||
Κατά τη δεκαετία του 1950, ο Σουηδός ιατρός Arvid Carlsson (Uppsala, University of Gothenburg, Σουηδία, 1923), ένας ερευνητής φαρμακευτικών ουσιών δοκίμασε την L-DOPA σε ζώα που παρουσίαζαν τα κλασικά συμπτώματα της νόσου του Parkinson και παρατήρησε δραστική μείωση των συμπτωμάτων με ταυτόχρονη βελτίωση στην υγεία τους.
Το 1957, ο Carlsson διαπίστωσε για πρώτη φορά τη σχέση σχιζοφρένειας και της νόσου του Parkinson. Κατά τη μελέτη της δράσης της ντοπαμίνης σε παρκινσονικούς ασθενείς διαπίστωσε ότι όταν αυτοί έπαιρναν υπερβολικές δόσεις του νευροδιαβιβαστή, εμφάνιζαν έντονα ψυχωτικά φαινόμενα. Η παρατήρηση αυτή οδήγησε στη διατύπωση της άποψης ότι η υπερβολική ντοπαμίνη στον εγκέφαλο αποτελεί μια από τις αιτίες της σχιζοφρένειας (ντοπαμινική υπόθεση για τη σχιζοφρένεια). Πράγματι, σε πολλές περιπτώσεις σχιζοφρενικών διαταραχών διαπιστώθηκε υπερβολική έκλυση ντοπαμίνης στις νευρικές συνάψεις, με αποτέλεσμα ο ερεθισμός να γίνεται αντιληπτός ως πολύ δυνατός.
Στις έρευνες του Carlsson που ακολούθησαν και σύντομα επεκτάθηκαν σε πολλά ερευνητικά κέντρα των ΗΠΑ, παρατηρήθηκε ότι το L-DOPA θεραπεύει τα συμπτώματα της νόσου του Parkinson. Συγχρόνως, διατυπώθηκε η υπόθεση ότι η σχιζοφρένεια είναι αποτέλεσμα της παρουσίας υπερβολικών ποσοτήτων ντοπαμίνης στον εγκέφαλο. Οι έρευνες αυτές οδήγησαν στην ανακάλυψη πολλών αντιψυχωτικών φαρμάκων και στον προσδιορισμό των εφαρμοζόμενων δοσολογιών.
Κατά την ίδια περίοδο, ο Carlsson ανέπτυξε μέθοδο μέτρησης της ντοπαμίνης στους ιστούς του εγκεφάλου και διαπίστωσε την ιδιαίτερη σημασία της συγκέντρωσής της στα βασικά γάγγλια (basal ganglia) του εγκεφάλου, τα οποία επηρεάζουν την κινητικότητα του ανθρώπου. Στα πειράματα που ο Carlsson διεξήγαγε με πειραματόζωα, χρησιμοποιούσε το ινδολικό αλκαλοειδές ρεζερπίνη (reserpine), ένα ισχυρό ηρεμιστικό φάρμακο, για να καταστείλει την παραγωγή ντοπαμίνης και στη συνέχεια χορηγούσε L-DOPA, η οποία ανέτρεπε τα δυσμενή αποτελέσματα της έλλειψης ντοπαμίνης. Με βάση αυτά τα πειράματα και άλλοι επιστήμονες άρχισαν να χορηγούν την L-DOPA για τη συμπτωματική θεραπεία σε παρκινσονικούς ασθενείς.
Για την έρευνα αυτή και τη μελέτη των θεραπευτικών ιδιοτήτων της ουσίας L-DOPA στη νόσο του Parkinson, ο Carlsson βραβεύθηκε με το Βραβείο Νόμπελ Ιατρικής και Φυσιολογίας το 2000. Μαζί με αυτόν βραβεύθηκαν και οι ιατροί Eric Kandel (Centre of Neurobiology and Behavior, Columbia University, New York) και Paul Greengard (Laboratory Molecular and Cellular Science, Rockfeller University, New York) "για τις ανακαλύψεις τους σχετικά με τη μεταγωγή σημάτων στο νευρικό σύστημα".
Κουνέλια στα οποία χορηγήθηκε ρεζερπίνη (ενδοφλεβίως, 5 mg/kg) και στη συνέχεια D,L-DOPA (ενδοφλεβίως, 200 mg/kg) [πηγή].
|
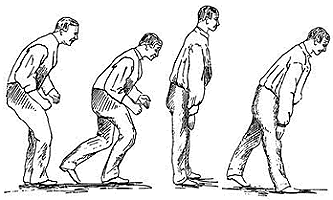
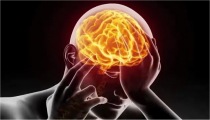
Λίγα στοιχεία για τη νόσο του Parkinson [Αναφ. 4] Η νόσος του Parkinson (Parkinson's disease), γνωστή και ως τρομώδης παράλυση (shaking pulsy), είναι μια εκφυλιστική νόσος του κεντρικού νευρικού συστήματος. Χαρακτηρίζεται από μια δυσχέρεια της κινητικότητας, όπως και από αμιμία, δηλ. ανέκφραστο πρόσωπο και μια γενικευμένη αδυναμία έκφρασης με χειρονομίες και βραδυψυχισμό, δηλ. αργή κίνηση, σκέψη και ομιλία. Οι ασθενείς παρουσιάζουν μια γενικευμένη δυσκολία στην κίνηση και όταν περπατούν, κάνουν μικρά, αργά και συρτά βήματα με το σώμα τους να παρουσιάζει μια κυρτή στάση. Κατά τη βάδιση, μπορούν εύκολα να χάσουν την ισορροπία τους και ιδιαίτερα όταν προσπαθήσουν να αλλάξουν κατεύθυνση. Χαρακτηριστικό σύμπτωμα είναι ο τρόμος (τρεμούλιασμα) στα χέρια και τα πόδια. ʼλλα, μη κινητικά συμπτώματα της νόσου, τα οποία συνήθως αποτελούν και τις αρχικές ενδείξεις της νόσου, είναι: η κατάθλιψη, οι διαταραχές ύπνου, οι οπτικές, ακουστικές και οσφρητικές ψευδαισθήσεις και η εύκολη κόπωση. Η άνοια είναι ένα από τα τελικά συμπτώματα της νόσου. Η νόσος του Parkinson είναι γνωστή από την αρχαιότητα. Η παλαιότερη περιγραφή της βρίσκεται σε μια βέδα (ιερό βιβλίο) των αρχαίων Ινδιών με το όνομα Kampa Vata (τρεμούλιασμα που έχει σχέση με τα νεύρα). Είναι χαρακτηριστικό το γεγονός ότι οι αρχαίοι Ινδοί είχαν βρει μια μέθοδο συμπτωματικής θεραπείας της νόσου, η οποία βασιζόταν στην κατανάλωση των σπερμάτων ενός τροπικού φυτού (Mucuna Prurien), που είναι ιδιαίτερα πλούσιο σε L-DOPA. Η ίδια νόσος είχε περιγραφεί και από πολλούς διάσημους ιατρούς, φαρμακοποιούς και ιατροφιλόσοφους της Ελληνορωμαΐκής εποχής (Διοσκουρίδης, Γαληνός, Κέλσος), όπως και αργότερα από τον διάσημο Πέρση ιατροφιλόσοφο και "πολυεπιστήμονα" Αβικέννα (Ibn Sina Avicenna).
Κατά την πιο σύγχρονη εποχή, το 1817, ο 'Aγγλος ιατρός James Parkinson (1755 - 1824) στη δημοσίευσή του "An Essay on the Shaking Palsy" περιέγραψε με ακρίβεια τα συμπτώματα της νόσου, στην οποία έδωσε τον επιστημονική ονομασία paralysis agitans, που στα ελληνικά αποδίδεται ως ''τρομώδης παράλυση''. Το 1862, η νόσος ονομάστηκε από τον διάσημο Γάλλο νευρολόγο Jean-Martin Charcot (1825 - 1893) νόσος του Parkinson ή Παρκινσονισμός , ονομασία η οποία από τότε έχει καθιερωθεί διεθνώς. Η νόσος προσβάλει περίπου το 0,2-0,3% του γενικού πληθυσμού, το 1% του πληθυσμού με ηλικία μεγαλύτερη των 65 ετών, ενώ έχει εκτιμηθεί ότι σημαντικό ποσοστό (5-10%) των ασθενών έχει αρχίσει να παρουσιάζει συμπτώματα της νόσου σε ηλικίες κάτω των 40 ετών (νεανικός παρκινσονισμός). Η νόσος του Parkinson είναι η 2η σε συχνότητα νευροεκφυλιστική νόσος, μετά τη νόσο Alzheimer. Μόνο σε μικρό ποσοστό ασθενών εμφανίζεται η νόσος λόγω κληρονομικότητας (οικογενής παρκινσονισμός). Η νόσος προσβάλει τους άνδρες σε διπλάσιο ποσοστό απ όσο τις γυναίκες.
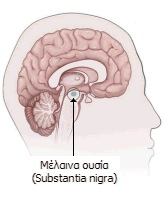
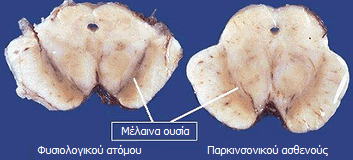
Η νόσος του Parkinson είναι μια χρόνια εξελισσόμενη και ιδιοπαθής νόσος, δηλαδή νόσος που δεν οφείλεται σε συγκεκριμένα παθολογικά αίτια και δεν είναι αποτέλεσμα κάποιας άλλης νόσου ή κάκωσης. Η βλάβη στην οποία οφείλονται τα συμπτώματα της νόσου εντοπίζεται σε μια δομή του εγκεφάλου με κύτταρα χαρακτηριστικού μαύρου χρώματος, που είναι γνωστή ως μέλαινα ουσία (substantia nigra) και βρίσκεται στον μίσχο του εγκεφάλου. Τα κύτταρα της μέλαινας ουσίας δημιουργούν στον εγκέφαλο την ουσία ντοπαμίνη, έναν νευροδιαβιβαστή, δηλ. μιας ουσίας μέσω της οποίας πραγματοποιείται η επικοινωνία μεταξύ των νευρικών κυττάρων στις περιοχές των συνάψεών τους (για τους νευροδιαβιβαστές, βλ. Χημική ένωση του μήνα: Νικοτίνη). Η απουσία ντοπαμίνης στην περιοχή της μέλαινας ουσίας οδηγεί στα χαρακτηριστικά συμπτώματα της νόσου του Parkinson. Διαπιστώθηκε ότι στους παρκινσονικούς ασθενείς η περιοχή της μέλαινας ουσίας έχει χάσει τη μαύρη χρωστική της, νευρομελανίνη (neuromelanin). Αυτό δεν οφείλεται σε κάποια κακή λειτουργία των κυττάρων που οδηγεί στην απώλεια της χρωστικής, αλλά στην ατροφία ή και την απουσία πολλών από αυτά. Με την πάροδο του χρόνου και σε φυσιολογικές σωματικές συνθήκες, τα κύτταρα εξαφανίζονται σταδιακά απ' την περιοχή της μέλαινας ουσίας. Ωστόσο, κατά την ασθένεια του Parkinson, για κάποιους μέχρι στιγμής απροσδιόριστους λόγους, τα κύτταρα αυτά ατροφούν ή χάνονται ή ατροφούν ταχύτερα, με συνέπεια την πρόωρη εμφάνιση των τυπικών συμπτωμάτων γήρανσης.
Παράγοντες, όπως η ψυχολογική καταπίεση (στρες) που υφίστανται ένα άτομο κατά τη διάρκεια της ζωής ή μια μακροχρόνια περίοδος κατάθλιψης, αυξάνουν την έκκριση ντοπαμίνης (ως άμυνα του οργανισμού), η οποία με τη σειρά της επιταχύνει τον σχηματισμό νευρομελανίνης στα συγκεκριμένα κύτταρα. Μελέτες έδειξαν ότι τα κύτταρα τα οποία περιέχουν αυξημένες ποσότητες νευρομελανίνης, είναι και τα πρώτα που καταστρέφονται. Πάντως, η συχνότητα εμφάνισης της νόσου δεν αυξάνει με την αύξηση της ηλικίας, όπως αρχικά πίστευαν. Οι σύγχρονες θεραπείες αποβλέπουν στον περιορισμό των πρώιμων κινητικών συμπτωμάτων της νόσου, κυρίως με τη χορήγηση L-DOPA (λεβοντόπα) και άλλων περιφερικών ντοπαμινικών αγωνιστών (dopaminc agonists). Ωστόσο, καθώς η νόσος εξελίσσεται και οι ντοπαμινεργικοί νευρώνες (dopaminergic neurons) συνεχίζουν να καταστρέφονται, τα φάρμακα αυτά σταδιακά αποτυγχάνουν και συγχρόνως προκαλούν τις χαρακτηριστικές ταχείες εναλλαγές της ψυχοκινητικής διάθεσης (φαινόμενο on-off). 'Εχει αποδειχθεί ότι συγκεκριμένες δίαιτες και ορισμένοι τύποι φυσικοθεραπείας απαλύνουν τα συμπτώματα της νόσου. Χειρουργικές επεμβάσεις, καθώς και ο "εν τω βάθει" εγκεφαλικός ερεθισμός μπορούν να μειώσουν τα συμπτώματα σε σοβαρές περιπτώσεις, όπου τα φάρμακα αποτυγχάνουν. Σήμερα, θεωρείται πλέον βέβαιο ότι δεν είναι μόνο η μέλαινα ουσία του εγκεφάλου το σημείο το οποίο προσβάλλει η νόσος. Η μεγάλη ποικιλία των συμπτωμάτων της, όπως π.χ. οι διαταραχές στην όσφρηση, στο πεπτικό σύστημα και στην ισορροπία, υποδηλώνουν ότι η νόσος προσβάλλει και άλλα κέντρα του εγκεφάλου. Οι νεότερες έρευνες αποβλέπουν στη θεραπεία της νόσου και όχι μόνο των συμπτωμάτων της. Ερευνούνται θεραπευτικά σχήματα βασιζόμενα στη γονιδιακή θεραπεία καθώς και σε μεταμοσχεύσεις βλαστοκυττάρων και νευροπροστατευτικών παραγόντων. Εικάζεται μια αποτελεσματικότητα των σχημάτων αυτών στα πολύ πρώιμα στάδια της νόσου, πριν ακόμη εμφανιστούν τα πρώτα συμπτώματα. Δυστυχώς όμως, δεν έχουν βρεθεί μέχρι σήμερα βιοχημικοί δείκτες (markers) προειδοποιητικοί της νόσου. Υπάρχουν επίσης φαρμακευτικές αγωγές για τα μη-κινητικά συμπτώματα της νόσου, όπως οι διαταραχές του ύπνου και άλλα ψυχιατρικά συμπτώματα. Στις προσπάθειες ενημέρωσης του κοινού περιλαμβάνεται και η καθιέρωση της 11ης Απριλίου ως διεθνούς ημέρας επαγρύπνησης για τη νόσο του Πάρκινσον με σύμβολο την κόκκινη τουλίπα. |
|||||||||||
Σύνθεση της L-DOPA [Αναφ. 5]
'Οπως προαναφέρθηκε, η σύνθεση της ρακεμικής 3,4-διυδροξυφαινυλαλανίνης (D,L-DOPA) πραγματοποιήθηκε για πρώτη φορά από τον Πολωνό βιοχημικό Casimir Funk (1884-1967), στα πλαίσια μια μελέτης αναζήτησης των πρόδρομων ενώσεων της αδρεναλίνης. Από τότε έχουν προταθεί αρκετές χημικές μέθοδοι σύνθεσης της D,L-DOPA.
Ενδεικτικά, μια σχετικά απλή μέθοδος (Barry, Mattocks, Hartung, 1948) ξεκινάει με πρώτη ύλη την πιπερονάλη η οποία εύκολα μπορεί να απομονωθεί από φυσικές ύλες. Το συνθετικό σχήμα βασίζεται στην αντίδραση συμπύκνωσής της με μηλονικό διαιθυλεστέρα, την αντίδραση του προϊόντος με νιτρώδη εστέρα και την αναγωγή της παραγόμενης οξίμης. Στη συνέχεια διασπάται η μεθυλενοδιοξυ-ομάδα με επίδραση υδροϊωδικού οξέος αποκαλύπτοντας τα δύο φαινολικά υδροξύλια. Η σύνθεση αυτή αποδίδεται συνοπτικά από την ακόλουθη σειρά αντιδράσεων:
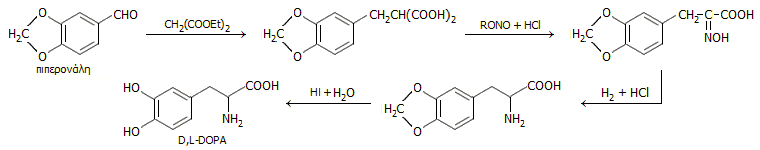
Αυτές οι "καθαρά χημικές" συνθέσεις αναπόφευκτα οδηγούν σε ρακεμικά μίγματα (ισομοριακά μίγματα D- και L-DOPA) τα οποία δύσκολα διαχωρίζονται σε οπτικούς αντίποδες. Το 1931, αναφέρθηκε ο πρώτος διαχωρισμός της D,L-DOPA στους οπτικούς αντίποδές της και βασιζόταν στον διαχωρισμό των αλάτων της πλήρως ακετυλιωμένης DOPA με το αλκαλοειδές βρυκίνη (Harington, Randal, 1931).
Η έρευνα έδειξε ότι η D-DOPA (dextrodopa) δεν παρουσιάζει κάποια ευεργετική βιοχημική δράση για τη νόσο του Parkinson, ως μη διασπώμενη ενζυματικώς προς ντοπαμίνη. Αντίθετα μάλιστα, η D-DOPA εμφανίζει μεγαλύτερη τοξικότητα από την L-DOPA, προφανώς λόγω αδυναμίας των ενζύμων του οργανισμού να την εξουδετερώσουν σχηματίζοντας αδρανή παράγωγά της. Πολλές από τις πρώτες φαρμακολογικές μελέτες διεξήχθησαν με συνθετική D,L-DOPA, η οποία όμως είχε προφανώς τη μισή δραστικότητα έναντι της νόσου του Parkinson από εκείνη της καθαρής L-DOPA, ενώ διατηρούσε τις ίδιες έως και εντονότερες τοξικές ιδιότητες. 'Ηταν προφανές ότι έπρεπε να αναζητηθούν μέθοδοι εύκολης παρασκευής του καθαρού και βιοχημικώς ενεργού L-εναντιομερούς, δηλ. της L-DOPA.
Μέθοδος Monsanto. Το 1983, η L-DOPA αποτέλεσε το "μοντέλο-στόχο" εναντιοεκλεκτικής κατάλυσης, δηλ. μιας αντίδρασης (εδώ υδρογόνωσης) μιας μη χειρόμορφης ένωσης, η οποία καταλύεται από χειρόμορφο καταλύτη, παρέχοντας ένωση με χειρόμορφο κέντρο (ασύμμετρο άτομο άνθρακα) με άνιση αναλογία οπτικών αντιπόδων.
Στην εναντιοεκλεκτική κατάλυση βασίζεται η βιομηχανική μέθοδος σύνθεσης L-DOPA, της εταιρίας Monsanto, όπου ως πρώτη ύλη χρησιμοποιείται η βανιλίνη (βλ. χημική ένωση του μήνα: Βανιλίνη). Η βανιλίνη αντιδρά με την N-ακετυλιωμένη γλυκίνη παρέχοντας ένα ακόρεστο παράγωγο. Το παράγωγο αυτό υπόκειται σε εναντιοεκλεκτική ή "ασύμμετρη" υδρογόνωση, οπότε λαμβάνεται σχεδόν αποκλειστικά το L-παράγωγο της L-DOPA με ee = 95% (ee: περίσσεια εναντιομερούς, enantiomeric excess), το οποίο με όξινη υδρόλυση παρέχει καθαρή L-DOPA. H σύνθεση συνοπτικά περιγράφεται από την ακόλουθη σειρά αντιδράσεων:
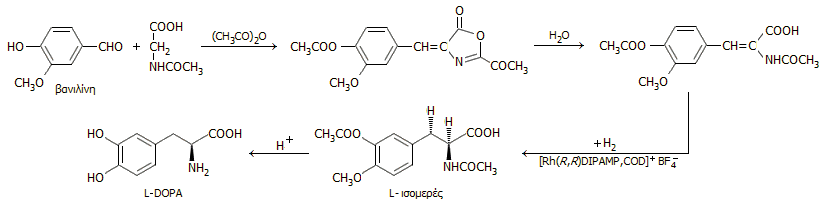
Ο καταλύτης που χρησιμοποιείται στο στάδιο της υδρογόνωσης (ομοιογενής κατάλυση) είναι ένα χειρόμορφο μικτό σύμπλοκο του ροδίου με έναν οργανοφωσφορικό (παράγωγo της φωσφίνης, PH3) υποκαταστάτη (DiPAMP), ο οποίος περιέχει δύο ασύμμετρα κέντρα (R, R), το [Rh(COD)(R,R-DiPAMP)] και ένα κυκλικό διένιο, το 1,5-κυκλοοκταδιένιο (COD).
 |
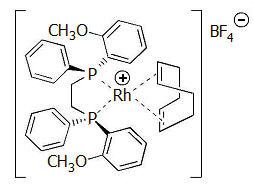 |
|
Αριστερά: Ο William Standish Knowles (1917-2012, βραβείο Nobel 2001). Δεξιά: Το μικτό σύμπλοκο του ροδίου που χρησιμοποιήθηκε ως καταλύτης για τη σύνθεση της L-DOPA. |
|
Για τη μέθοδο της εναντιοεκλεκτικής κατάλυσης αντιδράσεων υδρογόνωσης, ο Αμερικανός χημικός της εταιρίας Monsanto William Standish Knowles (1917-2012) και ο Ιάπωνας χημικός Ryōji Noyori (1938-), τιμήθηκαν με το ήμισυ του Βραβείου Nobel Χημείας του 2001 ("για την εργασία τους πάνω στις χειρομορφικώς καταλυόμενες αντιδράσεις υδρογόνωσης"). Με το υπόλοιπο ήμισυ του βραβείου Nobel τιμήθηκε ο Αμερικανός χημικός Karl Barry Sharpless (1941-) "για την εργασία του πάνω στις χειρομορφικώς καταλυόμενες αντιδράσεις οξείδωσης".
Βιοτεχνολογικές μέθοδοι. Το 2005, η ετήσια παγκόσμια παραγωγή L-DOPA έφτανε τους 250 τόνους εμπορικού όγκου 101 δισεκατομμυρίων (;) δολαρίων [Σημ. οι αναφερόμενες ποσότητες εγείρουν ερωτηματικά ως προς την ορθότητά τους. Αναφέρονται ως έχουν σε πολλές εργασίες σε έγκυρα επιστημονικά περιοδικά, ενδεχομένως όμως πρόκειται για λάθος που περνάει από δημοσίευση σε δημοσίευση (με παραπομπές στην Αναφ. 5θ), αν ληφθεί υπόψη ότι το κόστος της L-DOPA βρίσκεται στην περιοχή των 0,5-2$/g, ανάλογα με την ποσότητα, καθαρότητα και προέλευση].
|
Σκεύασμα ης Mucuna Pruriens και σπέρματα του φυτού γνωστά ως "βελούδινα σπέρματα" (velvet beans). |
Η μισή περίπου ποσότητα παραγόταν με ενζυματικές μεθόδους παρασκευή L-DOPA με ενζυματικές μεθόδους, με βάση την οξείδωση του αμινοξέος L-τυροσίνη με τη βοήθεια του ενζύμου τυροσινάση (tyrosinase).
'Εχει προταθεί μεγάλος αριθμός βιοτεχνολογικών μεθόδων, όπου χρησιμοποιούνται διάφοροι μικροοργανισμοί γενετιdκά τροποποιημένοι ή όχι για την παραγωγή L-DOPA με όσο το δυνατόν μικρότερο κόστος και μεγαλύτερη καθαρότητα.
Ιδιαίτερο ενδιαφέρον παρουσιάζει η δυνατότητα παραλαβής L-DOPA από καλλιέργειες κυττάρων φυτών, τα οποία είναι γνωστά για την ιδιαίτερα μεγάλη περιεκτικότητά τους σε L-DOPA. Το σπουδαιότερο από αυτά είναι το τροπικό φυτό Mucuna Pruriens, που, όπως προαναφέρθηκε, ήταν γνωστό ήδη από την αρχαιότητα στους Ινδούς για τις φαρμακευτικές ιδιότητές του. Σκευάσματα του φυτού διατίθενται στο εμπόριο, ως αντιπαρκινσονικά φάρμακα και γενικότερα ως θεραπευτικά νόσων του νευρικού συστήματος. Στα σκευάσματα αυτά συχνά αναφέρονται περιεκτικότητες L-DOPA που φθάνουν το 60-90%. Σχετικά πρόσφατα (2013), δημοσιεύθηκε άρθρο ανασκόπησης πάνω στις βιολογικές πηγές L-DOPA [Αναφ. 5ιγ].
Τέλος θα πρέπει να αναφερθεί ότι σκευάσματα της Mucuna Pruriens διατίθενται και στο εμπόριο (κυρίως μέσω του διαδικτύου) ως διατροφικά συμπληρώματα με τους εμπορικώς ελκυστικούς χαρακτηρισμούς "χαλαρωτικά", "βελτιωτικά της διάθεσης", "αφροδισιακά" και άλλους ανάλογους, που ωστόσο δεν υποστηρίζονται από τις κρατικές υπηρεσίες ελέγχου τροφίμων και φαρμάκων.
Βιοσύνθεση και μεταβολισμός της L-DOPA [Αναφ. 6]
Η L-DOPA παράγεται από το αμινοξύ L-τυροσίνη με την επίδραση του ενζύμου τυροσινάση, μια υδροξυλάση αρωματικών αμινοξέων. Να σημειωθεί ότι η L-τυροσίνη είναι μη απαραίτητο αμινοξύ (από τα 21 που συνθέτουν τις πρωτεΐνες) δεδομένου ότι μπορεί να συντεθεί στον οργανισμό από τη L-φαινυλαλανίνη, η οποία είναι απαραίτητο αμινοξύ και πρέπει να λαμβάνεται από την τροφή. Αποτελεί την πρόδρομη ένωση μονοαμινικών και κατεχολαμινικών νευροδιαβιβαστών, όπως η ντοπαμίνη, η νοραδρεναλίνη (νορεπινεφρίνη) και η αδρεναλίνη (επινεφρίνη). Η βιοσύνθεση των ενώσεων αυτών στο ανθρώπινο σώμα περιγράφεται από το ακόλουθο συνοπτικό σχήμα:
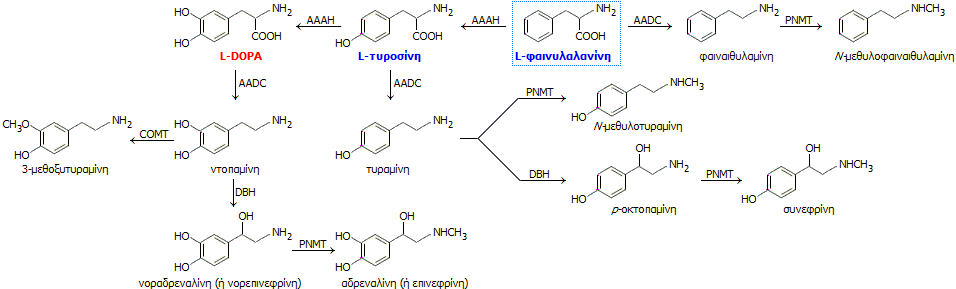
|
Βιοσuνθετική πορεία L-DOPA και άλλων κατεχολαμινών, όπως και ιχνοποσοτήτων άλλων αμινών στον ανθρώπινο οργανισμό από τα φυσικά αμινοξέα L-τυροσίνη και L-φαινυλαλανίνη. AAAH: υδροξυλάση αρωματικών αμινοξέων (aromatic amino acid hydroxylase), AADC: αποκαρβοξυλάση αρωματικών L-αμινοξέων (aromatic-L-amino acid decarboxylase), COMT: κατεχολική Ο-μεθυλοτρανσφεράση (catechol-O-methyltransferase). DBH: ντοπαμινική βητα-μονοοξυγενάση (dopamine beta-monooxygenase), PNMT: φαινυλαιθυλαμινο-Ν-μεθυλοτρανσφεράση (phenylethylamine N-methyltransferase) [πηγή]. |
Η κύρια μεταβολική πορεία της L-DOPA στον οργανισμό οδηγεί στον σχηματισμό της μελανίνης (melanin), μιας χρωστικής μαύρης ουσίας (ορθότερα: ομάδας ουσιών παρόμοιας δομής) πολυμερούς φύσης στην οποία οφείλεται ο χρωματισμός του δέρματος. Ο κύριος ρόλος της μελανίνης είναι η προστασία των κυττάρων από την υπεριώδη ακτινοβολία από τον ήλιο. Η βασική σειρά αντιδράσεων που οδηγεί από την L-DOPA στη μελανίνη (μια από τις πολλές μορφές της) μπορεί να αποδοθεί από την ακόλουθη σειρά αντιδράσεων.
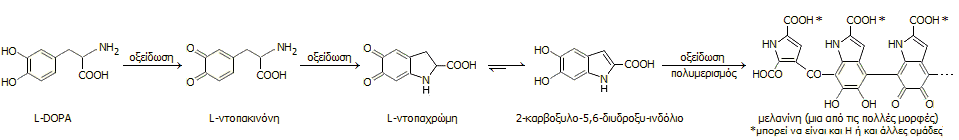
Στους παρκινσονικούς ασθενείς, λόγω των μεγάλων ποσοτήτων της χορηγούμενης L-DOPA καθίσταται σημαντική και μια δευτερεύουσα μεταβολική πορεία της ένωσης που περιγράφεται από το ακόλουθο σχήμα:
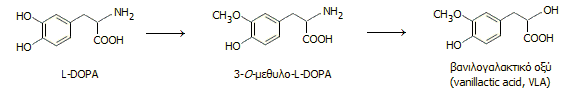
|
Δευτερεύουσα μεταβολική πορεία της L-DOPA, που είναι σημαντική στην περίπτωση χορήγησης L-DOPA σε παρκινσονικούς ασθενείς. Για να περιοριστεί η απώλεια της L-DOPA με τη μετατροπή της στο Ο-μεθυλοπαράγωγο συγχορηγούνται αναστολείς του σχετικού ενζύμου (Ο-μεθυλοτρανσφεράση). |
Η L-DOPA (λεβοντόπα) ως το κύριο φάρμακο για τη νόσο του Parkinson [Αναφ. 7]
Το 1960, ο Πολωνός Oleh Hornykiewicz (1926-) δοκίμασε για πρώτη φορά την L-DOPA σε παρκινσονικούς ασθενείς σε συνδυασμό με έναν αναστολέα της μονοαμινικής οξειδάσης, που σκοπό είχε τη μείωση της οξείδωσης της παραγόμενης ντοπαμίνης. Ωστόσο, τα αποτελέσματα ήταν περιορισμένα σε διάρκεια. Κατά την ίδια δεκαετία, ο 'Eλληνας ιατρός-φαρμακολόγος Γεώργιος Κοτζιάς (George Cotzias, 1918-1977) εργαζόταν σε ερευνητικό πολιτειακό εργαστήριο στο Long Island στην πολιτεία της Νέας Υόρκης. Η έρευνά του είχε σχέση με τις φαρμακολογικές και κλινικές ιδιότητες της L-DOPA και άλλων φαρμάκων σε παρκινσονικούς ασθενείς.
 |
 |
 |
|
Από αριστερά προς τα δεξιά: Oleh Hornykiewicz, 1926, Γεώργιος Κοτζιάς (George Cotzias, 1918-1977), Melvin Yahr (1917-2004). Οι τρεις αυτοί επιστήμονες μαζί, με τον νομπελίστα Arvid Carlsson, θεωρούνται η τετράδα των πρωτοπόρων της συμπτωματικής θεραπείας της νόσου του Parkinson με την L-DOPA [Αναφ. 7α]. |
||
Μέχρι το 1967, οι νευρολόγοι είχαν απογοητευτεί με τα αποτελέσματα των μελετών με την L-DOPA. Ωστόσο, τα πράγματα άλλαξαν όταν ο Κοτζιάς παρουσίασε τα αποτελέσματά του. Πίστευε ότι η νόσος του Parkinson οφειλόταν στην απώλεια της μέλαινας ουσίας από τον εγκέφαλο και αποφάσισε να καταβάλει προσπάθειες αναπλήρωσής της. Δοκίμασε διάφορες ουσίες μεταξύ των τη συνθετική DOPA (D,L-DOPA).
Ο Κοτζιάς άρχιζε τη χορήγηση συνθετικής DOPA σε μικρές δόσεις από το στόμα, τις οποίες αύξανε ανά δύο ώρες με συνεχή παρακολούθηση του ασθενή. Αυτός ο τρόπος χορήγησης περιόριζε τα γαστροεντερικά προβλήματα. Οι δόσεις έφθαναν και τα 12 g/ημέρα, ενώ η βελτίωση των ασθενών ήταν δραματική. Αυτή υπήρξε η αρχή της αποτελεσματικής συμπτωματικής θεραπείας της νόσου με την L-DOPA.
'Eνας άλλος ερευνητής, o κλινικός νευρολόγος Melvin Yahr (1917-2004) πραγματοποίησε παρόμοια πειράματα και αρχικά ήταν διστακτικός ως προς τη χορήγηση L-DOPA, όμως εντυπωσιάσθηκε όταν σε βίντεο είδε τον Κοτζιά να παρουσιάζει ασθενείς του, στους οποίους είχε χορηγήσει το φάρμακο.
Ο Yahr κατάλαβε ότι για την εξαγωγή οριστικών συμπερασμάτων ήταν απαραίτητη η διεξαγωγή μιας ελεγχόμενης διπλά-τυφλής κλινικής μελέτης (double-blind controlled clinical trial), δηλ. μιας μελέτης σε ομάδες ασθενών κατά την οποία δεν γνωρίζουν ούτε οι ασθενείς, ούτε οι παρακολουθούντες ιατροί σε ποιούς χορηγήθηκε το υπό μελέτη φάρμακο ή ένα εικονικό φάρμακο (placebo). Η μελέτη αυτή του Yahr, όπως και άλλες που ακολούθησαν απέδειξαν ότι η μέθοδος του Κοτζιά ήταν αποτελεσματική και τα συμπτώματα δυσκινησίας και o τρόμος εξαφανίζονταν συστηματικά με τη χορήγηση L-DOPA.
|
Η ντοπαμίνη είναι απαραίτητος νευροδιαβιβαστής για την επικοινωνία των νευρώνων. Κατά τη νόσο του Parkinson, μειώνεται ή παύει η παραγωγή ντοπαμίνης στον εγκέφαλο και δεν μπορεί να εισέλθει ντοπαμίνη από την περιφερική κυκλοφορία ντοπαμίνη προς αναπλήρωσή της, λόγω του αιματοεγκεφαλικού φραγμού. Αντίθετα, η L-DOPA διαπερνά τον φραγμό και εισέρχεται στον εγκέφαλο, όπου διασπάται ταχέως παρέχοντας την απαραίτητη για την επικοινωνία των νευρώνων ντοπαμίνη. |
Το 1970, η Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (Food and Drug Administration, FDA) ενέκρινε τη χορήγηση της L-DOPA σε παρκινσονικούς ασθενείς. Ακολούθησαν βελτιώσεις στη δοσολογία, όπως και η χρήση συνδυασμένης φαρμακολογίας, δηλ. συνδυασμών L-DOPA με άλλα φάρμακα, οι οποίοι αποδείχθηκαν εξαιρετικά φάρμακα για τη θεραπεία των συμπτωμάτων της νόσου.
Δοσολογία. Η L-DOPA χαρακτηρίζεται από μια ιδιαίτερη φαρμακοκινητική και φαρμακοδυναμική. Χορηγείται σε τρεις, τέσσερις ή και παραπάνω δόσεις την ημέρα, ανάλογα με τις ανάγκες του αρρώστου. Η συμβατική δοσολογία της L-DOPA κυμαίνεται από 150 έως 1200 mg/ημέρα, ανάλογα με την περίπτωση και τα συνοδευτικά φάρμακα. Η πυριδοξίνη, μια μορφή της βιταμίνης Β6, δρα ως συμπαράγοντας (cofactor) και συνήθως συγχορηγείται με την L-DOPA.
Ο χρόνος λήψης του φαρμάκου σε σχέση με τα γεύματα, η συγχορήγηση της L-DOPA με άλλα φάρμακα, όπως επίσης η περιεκτικότητα των τροφών σε πρωτεΐνες, μπορούν να αυξήσουν ή να ελαττώσουν την αποτελεσματικότητά της. Ο χρόνος υποδιπλασιασμού (half life) της συγκέντρωσης της L-DOPA στο αίμα είναι σχετικά σύντομος: 60 έως 90 min.
Δυστυχώς, παρά τα θεαματικά αποτελέσματά της, η L-DOPA δεν ανακόπτει τη συνεχή απώλεια των νευρικών κυττάρων και επομένως την επιδείνωση των συμπτωμάτων της νόσου. Μάλιστα, συζητείται στη διεθνή βιβλιογραφία για το αν και κάτω από ποιες συνθήκες η ίδια η L-DOPA συνεισφέρει στον κυτταρικό θάνατο, όμως μέχρι στιγμής η επιστημονική κοινότητα δεν έχει καταλήξει σε σαφή συμπεράσματα ως προς αυτό το δυσάρεστο ενδεχόμενο.
Σε ασθενείς, οι οποίοι λαμβάνουν για μεγάλο χρονικό διάστημα υψηλές δόσεις L-DOPA, συχνά παρουσιάζονται παράδοξες ακούσιες κινήσεις καθώς και ημερήσιες διακυμάνσεις των συμπτωμάτων, που συχνά σχετίζονται με το δοσολογικό σχήμα. Σε κάθε περίπτωση, η δοσολογία είναι αυστηρά εξατομικευμένη και πρέπει να ρυθμίζεται αποκλειστικά από τον νευρολόγο που παρακολουθεί τον ασθενή.
Μηχανισμός δράσης. Η φαρμακευτική δράση της L-DOPA βασίζεται στη δυνατότητά της να διέλθει μέσω του αιματοεγκεφαλικού φραγμού (blood-brain barrier, BBB) και να εισέλθει στον εγκέφαλο, όπου υφίσταται αποκαρβοξυλίωση παρέχοντας ντοπαμίνη. Με τον τρόπο αυτό αναπληρώνονται οι ποσότητες ντοπαμίνης που αδυνατούν πλέον να παραχθούν στον εγκέφαλο στους παρκινσονικούς ασθενείς, λόγω της απουσίας ή του εκφυλισμού των κυττάρων της μέλαινας ουσίας (substantia nigra). Απευθείας χορήγηση ντοπαμίνης στους ασθενείς δεν είναι αποτελεσματική, δεδομένου ότι η ουσία αυτή δεν μπορεί να διαπεράσει τον αιματοεγκεφαλικό φραγμό και να εισέλθει στον εγκέφαλο από την περιφερική κυκλοφορία. Η δράση αυτή απεικονίζεται στο παραπλεύρως σχήμα.
Η L-DOPA βοηθά με θαυμάσιο τρόπο περίπου τα τρία τέταρτα των παρκινσονικών ασθενών, ωστόσο δεν αντιμετωπίζει με την ίδια αποτελεσματικότητα όλα τα συμπτώματα της νόσου. Για παράδειγμα, η βραδυκινησία και η δυσκαμψία υποχωρούν σε μεγάλο βαθμό, όμως ο τρόμος και τα προβλήματα ισορροπίας υποχωρούν σε μικρότερο βαθμό ή και καθόλου.
|
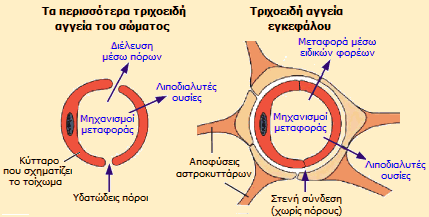
Αιματοεγκεφαλικός φραγμός [Αναφ. 8] Ο εγκέφαλος είναι το μόνο όργανο που διαθέτει το δικό του "σύστημα ασφαλείας". Τροφοδοτείται με τα απαραίτητα θρεπτικά συστατικά από πυκνό δίκτυο τριχοειδών αιμοφόρων αγγείων, τα οποία όμως δεν επιτρέπουν τη διέλευση ουσιών (τοξίνες, βακτήρια) που θα μπορούσαν να τον βλάψουν. Ο φραγμός αυτός είναι γνωστός ως αιματοεγκεφαλικός φραγμός (blood-brain barrier, BBB) και είναι τόσο αποτελεσματικός ως προς τον αποκλεισμό ξένων ουσιών, που συχνά αποκλείει και τη διέλευση φαρμακευτικών ουσιών οι οποίες θα διόρθωναν άλλες βλάβες του εγκεφάλου. Το 1885, ο Γερμανός ιατρός Paul Ehrlich (1854-1915), γνωστός για τη μετέπειτα (1909) ανακάλυψη του αρσενικούχου σκευάσματος salvarsan (το "ιστορικό" σκεύασμα 606) για τη σύφιλη, έκανε ένεση διαλύματος της χρωστικής "κυανούν του μεθυλενίου" σε ποντίκια. Στη συνέχεια, διαπίστωσε ότι όλοι οι ιστοί των πειραματόζωων είχαν είχαν χρωματισθεί κυανοί, με εξαίρεση τον εγκέφαλο, που διατηρούσε το φυσικό του χρώμα. Σε πειράματα που ακολούθησαν διαπιστώθηκε και το αντίστροφο. 'Ενεση της ίδιας χρωστικής στον εγκέφαλο, χρωμάτιζε τον εγκέφαλο και όχι κάποιον άλλο ιστό του σώματος. Τα πειράματα αυτά οδήγησαν στο συμπέρασμα της ύπαρξης κάποιου φυσικού φραγμού που διαχωρίζει τον εγκέφαλο από την κύρια κυκλοφορία του αίματος. Ωστόσο, τα μικροσκόπια εκείνης της εποχής δεν μπορούσαν να διακρίνουν κάποια διαφορά μεταξύ των τριχοειδών αιμοφόρων αγγείων του εγκεφάλου και εκείνων του υπόλοιπου σώματος.
Το 1960, με μικροσκόπια 5000 φορές ισχυρότερα από εκείνα της εποχής του Ehrlich, διευκρινίσθηκαν οι διαφορές στη φύση των τριχοειδών αιμοφόρων αγγείων του εγκεφάλου από τα αντίστοιχα αγγεία του σώματος. 'Οπως και τα άλλα αγγεία του σώματος, έτσι και εκείνα του εγκεφάλου φέρουν εσωτερικό χιτώνα από ενδοθηλιακά κύτταρα, τα οποία δρουν ως ενδιάμεση φάση μεταξύ κυκλοφορούντος αίματος και των τοιχωμάτων του αγγείου. Η διαφορά έγκειται στο ότι στα αγγεία του σώματος τα κύτταρα αυτά αφήνουν κενά μεταξύ τους (πόρους), ενώ στα αγγεία του εγκεφάλου τα αντίστοιχα κύτταρα έχουν πυκνή διάταξη και οι πόροι είναι σχεδόν κλειστοί.
Διαπιστώθηκε ότι ενώσεις με πολύ μικρά μόρια ή λιποδιαλυτά (π.χ. αντικαταθλιπτικά φάρμακα, αλκοόλη, διάφορες ναρκωτικές ουσίες και ορμόνες) μπορούν να διέλθουν μέσω του αιματοεγκεφαλικού φραγμού. Για παράδειγμα, η ηρωίνη (ακετυλιωμένη μορφίνη) είναι πιο δραστική σε σχέση με τη μορφίνη, επειδή διαπερνά τον αιματοεγκεφαλικό φραγμό ευκολότερα λόγω μεγαλύτερης λιποφιλικότητας. Αντίθετα, υδατόφιλα μόρια (π.χ. γλυκόζη) μπορούν να διαπεράσουν τον αιματοεγκεφαλικό φραγμό με τη βοήθεια ορισμένων πρωτεϊνών. Είναι χαρακτηριστικό το ότι τα κύτταρα που βρίσκονται από τις δύο πλευρές του φραγμού "συνεννοούνται" μεταξύ τους ως προς το σε ποια μόρια θα επιτρέψουν τη διέλευση και πότε. Για παράδειγμα, αν ο εγκέφαλος εργάζεται εντατικά, τα αγγεία του θα διασταλούν, έτσι ώστε να ανοίξουν οι πόροι και να επιτραπεί η ταχεία διέλευση "ενεργειακών" συστατικών. 'Οταν ο φραγμός υποστεί βλάβη (π.χ. σε μια ασθένεια, φλεγμονή ή μετά από κάποιον τραυματισμό) είναι πιθανή η είσοδος στον εγκέφαλο επικίνδυνων ουσιών που θα προκαλέσουν σημαντικά προβλήματα και μολύνσεις. Η επιδιόρθωση των βλαβών αυτών, όπως και ο σκοπούμενος σχηματισμός ανοιγμάτων για τη διέλευση χρήσιμων ουσιών, αποτελεί ένα πρόβλημα πάνω στο οποίο διεξάγεται σημαντική έρευνα. Επίσης αναπτύσσονται στρατηγικές πρόσδεσης των φαρμακευτικών ουσιών με ουσίες-φορείς, που διέρχονται μέσω του φραγμού και οι οποίες θα δράσουν ως "δούρειοι ίπποι", βοηθώντας τις φαρμακευτικές ουσίες να εισέλθουν στον εγκέφαλο. |
||||||||
Παρενέργειες. Δυστυχώς η χορήγηση L-DOPA συνοδεύεται από πολλές παρενέργειες, όπως: ανορεξία, ναυτία, εμετοί και άλλες ενοχλήσεις στο πεπτικό σύστημα, κεφαλαλγία, υπόταση, καρδιακή αρρυθμία, αιματολογικές διαταραχές, αλωπεκία, εφιάλτες, υπνηλία, σύγχυση και ψύχωση με ψευδαισθήσεις, αντικοινωνική συμπεριφορά, αυξημένη libido.
Συνοδευτικές φαρμακευτικές ουσίες. Σήμερα, η L-DOPA (λεβοντόπα) σπάνια πλέον χορηγείται μόνη της. Συνήθως, χορηγείται ως μίγμα με άλλες φαρμακευτικές ουσίες (φάρμακα-"δορυφόροι") η παρουσία των οποίων έχει ως σκοπό την αποφυγή της μετατροπής της σε ντοπαμίνη ή σε άλλα παράγωγα πριν ακόμη αυτή φθάσει στον εγκέφαλο. 'Ετσι αυξάνεται η βιοδιαθεσιμότητα και ο χρόνος υποδιπλασιασμού της L-DOPA, περιορίζεται το μέγεθος των απαιτούμενων δόσεών της, εξοικονομούνται ποσότητές της και -κυρίως- αποφεύγεται η χορήγηση μεγάλων δόσεών της και επομένως περιορίζονται οι ανεπιθύμητες παρενέργειές της.
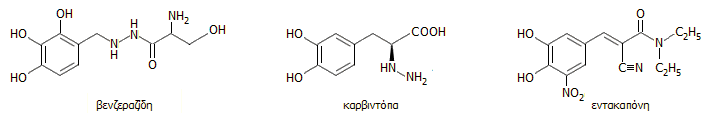
Η βενζεραζίδη (benserazide) και η καρβιντόπα (carbidopa) είναι οι κυριότερες από τις ουσίες που συνήθως συγχορηγούνται με την L-DOPA. Συνδυασμοί των ουσιών αυτών με την L-DOPA κυκλοφορούν με το εμπορικά ονόματα Madopar και Sinemet, αντιστοίχως. Οι ουσίες αυτές αναστέλλουν το ένζυμο αποκαρβοξυλάση της L-DOPA (DOPA decarboxylase, DDC), το οποίο προκαλεί την αποκαρβοξυλίωση της L-DOPA και αποφεύγεται η περιφερική -και επομένως πρόωρη- μετατροπή της σε ντοπαμίνη. Η μετατροπή αυτή αφενός διεγείρει τους περιφερικούς υποδοχείς ντοπαμίνης προκαλώντας ναυτία και εμετούς, αφετέρου μειώνει την ποσότητα L-DOPA που φθάνει στον εγκέφαλο.
Μια άλλη συνοδευτική ουσία είναι η εντακαπόνη (entacapone), μια νιτροκατεχόλη, η οποία δρα ως αναστολέας της κατεχολο-Ο-μεθυλο-τρανσφεράσης (catechol-O-methyl transferase, COMT), η οποία μεθυλιώνει το 3-υδροξύλιο της L-DOPA και ουσιαστικά την αχρηστεύει. Φαρμακευτικό σκεύασμα που συνδυάζει την L-DOPA με καρβιντόπα και εντακαπόνη κυκλοφορεί με την εμπορική ονομασία Stalevo.
|
Φαρμακευτικές ουσίες που χορηγούνται σε συνδυασμό με την L-DOPA (λεβοντόπα) για να αποφευχθεί η περιφερική αλλοίωσή της από διάφορα ένζυμα του οργανισμού και να μειωθεί έτσι το μέγεθος των απαιτούμενων δόσεων. Η βενζεραζίδη και η καρβιντόπα αναστέλλουν τα ένζυμα αποκαρβοξυλίωσης της L-DOPA, ενώ η εντακαπόνη αναστέλλει τη μεθυλίωση του 3-υδροξυλίου της. |
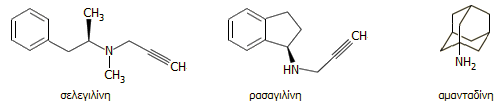
'Αλλα φάρμακα για τη νόσο του Parkinson που χρησιμοποιούνται μόνα τους ή σε συνδυασμό με την L-DOPA χρησιμοποιούνται οι αναστολείς της μονοαμινοξειδάσης τύπου Β [monoamine oxidase-B (MAO-B) inhibitors] σελεγιλίνη (selegilin) και ρασαγιλίνη (rasalgilin) με μια ενδιαφέρουσα από χημική άποψη ακετυλενική ομάδα στο μόριό τους. Τα φάρμακα αυτά προλαμβάνουν την οξειδωτική καταστροφή της ντοπαμίνης στον εγκέφαλο από το ένζυμο αυτό και αντισταθμίζουν έτσι τη μειωμένη παραγωγή της ντοπαμίνης, ιδιαίτερα στα πρώτα στάδια της νόσου του Πάρκινσον. 'Ενα αντιικό φάρμακο, η αμανταδίνη (amantadine), (με εμπορικό όνομα Symmetrel) είναι ένα παράγωγο του αδαμαντάνιου (1-αμινοαδαμαντάνιο) που χρησιμοποιείται επίσης για τη θεραπεία της νόσου του Πάρκινσον, αν και οι ενδείξεις ως προς την αποτελεσματικότητα και την ασφαλή χρήση του δεν έχουν κριθεί ως ικανοποιητικές.
|
Φαρμακευτικές ουσίες που χορηγούνται μόνες τους ή σε συνδυασμό με την L-DOPA (λεβοντόπα). Η σελεγιλίνη και η ρασαγιλίνη είναι αναστολείς της μονοαμινικής οξειδάσης Β και προλαμβάνουν την οξειδωτική καταστροφή της ντοπαμίνης στον εγκέφαλο. Η αμανταδίνη είναι ένα αντιικό φάρμακο που χορηγείται και σε παρκινσονικούς ασθενείς, αν και η αποτελεσματικότητά του αμφισβητείται. |
 |
 |
 |
 |
 |
 |
|
Διάφορα φαρμακευτικά σκευάσματα L-DOPA (λεβοντόπα). |
|||||
|
Γεώργιος Κοτζιάς [Αναφ. 9]
Ο Γεώργιος Κοτζιάς από πολλούς επιστήμονες θεωρείται πρωτοπόρος ερευνητής που προηγήθηκε της εποχής του, καθώς χάραξε νέους δρόμους στη νευροφυσιολογία του εγκεφάλου και προέβλεψε τη νευροβιολογική φαρμακευτική επανάσταση της εποχής μας και ιδιαίτερα της χρήσης ουσιών, όπως η L-DOPA. Γεννήθηκε στα Χανιά της Κρήτης στις 16 Ιουνίου 1918. 'Ηταν ο πρωτότοκος γιος του συντηρητικού πολιτικού και εκλεγμένου δημάρχου της Αθήνας Κωνσταντίνου Κοτζιά (δημαρχία 1934-36 και 1951). Φοίτησε στην Ιατρική Σχολή του Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών. Το 1941, όταν τα γερμανικά στρατεύματα κατοχής εισέβαλαν στην Ελλάδα, ως φοιτητής (στο 5ο έτος) διέφυγε με τους γονείς του στην Τουρκία και στη συνέχεια μέσω Αιγύπτου και Αφρικής, εγκαταστάθηκε στη Νέα Υόρκη όπου αντιμετώπισε πολλές βιοποριστικές δυσκολίες. Αρχικά, ο Γεώργιος Κοτζιάς υπέβαλε αιτήσεις σε διάφορες σχολές για να ολοκληρώσει τις σπουδές του στην ιατρική. Η αίτησή του απορρίφθηκε από την Ιατρική Σχολή του Cornell (Νέα Υόρκη) καθώς κρίθηκε ανεπαρκής ως προς τις γνώσεις του επί της αγγλικής γλώσσας, καθώς και ως προς την εκπαίδευσή του στη βασική βιοχημεία, τη φαρμακολογία και τη φυσιολογία, λόγω της ανώμαλης περιόδου. Ωστόσο, αποφασίζει να υποβάλλει αίτηση στη διάσημη Ιατρική Σχολή του Πανεπιστημίου Harvard και ο γερμανοαμερικανός καθηγητής Soma Weiss (πρόσφυγας και ο ίδιος από τη ναζιστική Γερμανία) μετά από μακρά συζήτηση μαζί του στα γερμανικά, τα οποία ο Κοτζιάς μιλούσε με ευχέρεια, του πρότεινε να εισαχθεί υπό όρους στο 3ο έτος σπουδών της Ιατρικής Σχολής. Δύο χρόνια αργότερα αποφοίτησε από το Harvard με πτυχίο "cum laude".
Μετά τη λήψη του πτυχίου της Iατρικής υπηρέτησε στο Γενικό Νοσοκομείο της Μασαχουσέτης (1944-46), στο Νοσοκομείο του Ινστιτούτου Ροκφέλερ (1946-50) και στο Εθνικό Συμβούλιο Ερευνών (1951-52). Τιμήθηκε με τέσσερις πανεπιστημιακούς τίτλους: καθηγητής της Iατρικής του Πανεπιστημίου της Πολιτείας της Νέας Υόρκης, καθηγητής της Nευρολογίας στην Ιατρική Σχολή του Mount Sinai, καθηγητής της Nευρολογίας στο Ιατρικό Κολέγιο του Cornell και καθηγητής της Ιατρικής του Πανεπιστημίου Ροκφέλερ. Επίσης, διετέλεσε ειδικός σύμβουλος-συνεργάτης του Καρκινολογικού Κέντρου Memorial Sloan-Kettering, καθώς και σύμβουλος-ερευνητής και διευθυντής του ιατρικού τμήματος και του ερευνητικού κέντρου του Brookhaven. Το πρωτότυπο συγγραφικό έργο του Γεωργίου Κοτζιά αποτελείται από 200 επιστημονικές δημοσιεύσεις, οι περισσότερες από τις οποίες έχουν δημοσιευθεί στα σπουδαιότερα ιατρικά περιοδικά του κόσμου (π.χ. New England Journal of Medicine). Υπήρξε ένας από τους πρώτους ερευνητές που προέβλεψαν την τεράστια κλινική και ερευνητική σημασία των ονομαζόμενων νευροδιαβιβαστών και των νευροπεπτιδίων, μελετώντας το μεταβολισμό διαφόρων βιογενών αμινών και αμινοξέων. Η εξακρίβωση του τρόπου δράσης της L-DOPA από τον Κοτζιά άνοιξε νέους ορίζοντες στην καταπολέμηση των συμπτωμάτων της νόσου του Parkinson, αφού μετά τις πρωτοποριακές δημοσιεύσεις του, άρχισε να χρησιμοποιείται στη θεραπευτική ένα πλήθος από άλλες παρεμφερείς ουσίες που μιμούνται τη δράση της ντοπαμίνης. Το πολυσήμαντο ερευνητικό έργο του Γεωργίου Κοτζιά αναγνωρίστηκε τόσο σε Ελλάδα, όσο και σε εξωτερικό. Στη χώρα μας εξελέγη αντεπιστέλλον μέλος της Ακαδημίας Αθηνών το 1971 και αναγορεύθηκε επίτιμος διδάκτορας της Ιατρικής Σχολής του Πανεπιστημίου Αθηνών το 1976, όπου, αν και βαριά άρρωστος, ανέπτυξε διεξοδικά το θέμα «Μακροζωία, εγκεφαλικαί εκφυλίσεις και αμίναι». Επίσης, τιμήθηκε από την ελληνική πολιτεία με τον τίτλο του Ανώτερου Ταξιάρχη του Φοίνικος το 1977. Ο Κοτζιάς, μαζί με τον κορυφαίο θεμελιωτή του κλάδου της αποφολιδωτικής κυτταρολογίας Γεώργιο Παπανικολάου υπήρξε ο πλέον πολυβραβευμένος 'Ελληνας ερευνητής του 20ου αιώνα έχοντας τιμηθεί επάξια με 22 επίζηλες διακρίσεις. Μεγαλύτερη διάκριση υπήρξε το έπαθλο Albert Lasker-DeBekay του1969. Δυστυχώς, ο Γεώργιος Κοτζιάς υπήρξε μανιώδης καπνιστής με αποτέλεσμα να προσβληθεί από καρκίνο των πνευμόνων. Το 1977 απεβίωσε πρόωρα σε ηλικία 59 ετών έχοντας αντιμετωπίσει την ασθένεια με αξιοζήλευτη γενναιότητα. 'Οταν πέθανε ήταν τακτικός καθηγητής της Νευρολογίας στο Ιατρικό Κέντρο του Cornell. To 2012, ο νευρολόγος Bernard Michael Patten συνέγραψε ένα εξαιρετικά τιμητικό βιβλίο (e-book) για τον Κοτζιά με τίτλο: "The Great Cotzias: Discoverer of the Treatment for Parkinsons Disease". |
|||||
 |
 |
 |
 |
 |
 |
|
Μερικά από τα πολλά βιβλία που έχουν κυκλοφορήσει για τη νόσο του Parkinson και τη θεραπεία με την L-DOPA. |
|||||
|
"Awakenings" μια κινηματογραφική ταινία σχετική με την L-DOPA [Αναφ. 10] To 1990 προβλήθηκε μια κινηματογραφική ταινία με τίτλο "Awakenings" (στην Ελλάδα προβλήθηκε με τον τίτλο "Ξυπνήματα") της οποίας το σενάριο βασιζόταν στο ομώνυμο βιβλίο του Βρετανού νευροχειρουργού Oliver Sacks (1933 - 2015), ο οποίος το εξέδωσε κατά το 1973 ως απομνημονεύματά του. Το βιβλίο αυτό έχει χαρακτηρισθεί ως "αριστούργημα". Στο βιβλίο και στην ταινία περιγράφεται μια πραγματική ιστορία που συνέβη κατά το 1969 και αφορούσε τη χορήγηση του τότε νέου φαρμάκου για τους παρκινσονικούς ασθενείς, της L-DOPA, για τη θεραπεία κατατονικών ασθενών. Οι περισσότεροι από τους ασθενείς αυτούς υπήρξαν θύματα μιας επιδημίας ληθαργικής εγκεφαλίτιδας (encephalitis lethargica) (γνωστής και ως νόσος Constantin von Economo), η οποία είχε παγκόσμια εξάπλωση κατά τη δεκαετία του 1920 και είχε προκαλέσει περισσότερους από ένα εκατομμύριο θανάτους. Σε όσους επέζησαν, η νόσος αυτή άφησε μόνιμες βλάβες στον εγκέφαλο ανάλογες με εκείνες που οδηγούν στη νόσο του Parkinson. Ο ιατρός πληροφορήθηκε σε ένα σεμινάριο τα αποτελέσματα της χορήγησης της L-DOPA στους παρκινσονικούς ασθενείς και θέλησε να το δοκιμάσει και στους κατατονικούς ασθενείς του. Στην αρχή, τα αποτελέσματα υπήρξαν εντυπωσιακά. Στην κυριολεξία, χάρις στο φάρμακο "ξύπνησαν" ασθενείς που βρίσκονταν σε κατάσταση κατατονίας για δεκαετίες. Δυστυχώς, σύντομα ο οργανισμός των ασθενών άρχισε να παρουσιάζει ανοχή στο φάρμακό. Το γεγονός αυτό ανάγκαζε τον ιατρό να χορηγεί συνεχώς αυξανόμενες δόσεις, οι οποίες έφτασαν πλέον σε τοξικά επίπεδα και προκαλούσαν άσχημες παρενέργειες (σπασμούς, παράνοια και βίαιη συμπεριφορά). Το τελικό αποτέλεσμα ήταν όλοι οι ασθενείς να επανέλθουν στην αρχική κατατονική κατάστασή τους.
Εκπληκτικές υπήρξαν οι ερμηνείες των ηθοποιών Robin Williams (στον ρόλο του νευροχειρουργού) και του Robert De Niro (στον ρόλο του ασθενούς). Η ταινία και οι πρωταγωνιστές της προτάθηκαν για πολλά βραβεία. Το 1991, οι δύο πρωταγωνιστές τιμήθηκαν με τα βραβεία "National Board of Review Awards" και "New York Film Critics Circle Awards". |
||||||