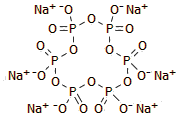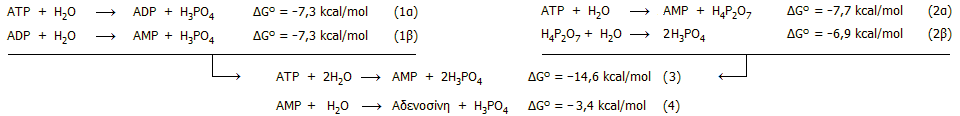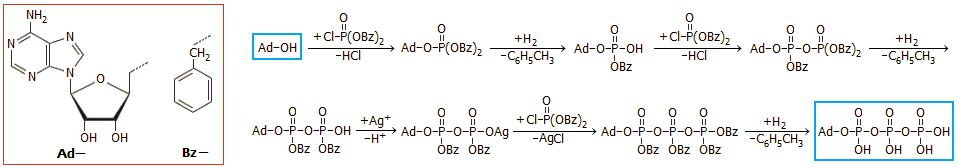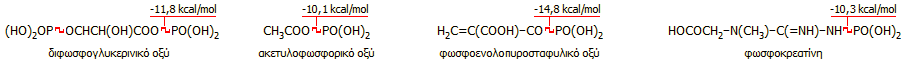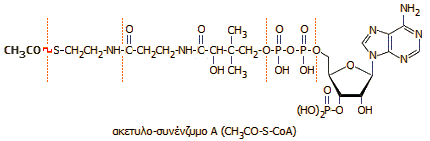Λίστα "Χημικών Ενώσεων του Μήνα"
Η χημική ένωση του
μήνα
[Μάιος - Ιούνιος
2013]
Επιμέλεια σελίδας:
Θανάσης Βαλαβανίδης, Καθηγητής
-
Κωνσταντίνος
Ευσταθίου, Καθηγητής
|
Φυσικoχημικές ιδιότητες
[Αναφ. 1]:
Εμφάνιση: 'Αμορφο (υαλώδες)
άχρωμο, στερεό
Μοριακός τύπος:
C10H16N5O13P3
Σχετική μοριακή μάζα:
507,18
Σημείο τήξεως
(το δινάτριο άλας):
187ºC (υπό αποσύνθεση)
Πυκνότητα (το
δινάτριο άλας): 1,04 g/cm3
Συντελεστής απορρόφησης, ε = 15,4x104 M-1cm-1
(259 nm),
pH διαλύματος 1%:
περίπου 2.
[α]D22
= -26,7º
(c = 3,095).
Η ένωση είναι εξαιρετικά ευδιάλυτη στο νερό.
Καθιζάνει ως τετραϋδρικό ή εξαϋδρικό άλας με Ba.
Ισχύς ως οξύ:
pKa1 = 4,31, pKa2 = 6,76 (25ºC, σε διάλυμα 0,10 Μ NaCl,
[Αναφ. 1γ]),
δηλ. δρα
ως ασθενές διπρωτικό οξύ. Αν και μπορεί να υποστεί περαιτέρω διάσταση,
αυτό προϋποθέτει αλκαλικό διάλυμα, όπου όμως η τριφωσφορική ομάδα θα υδρολυθεί.
Το υδατικό διάλυμά του είναι σταθερό στους
0ºC για αρκετές ώρες. Σταθερότερα είναι τα
υδατικά διαλύματά του, που περιέχουν ρυθμιστικό διάλυμα με pH στην
περιοχή 6,8-7,4.
|
 |
|
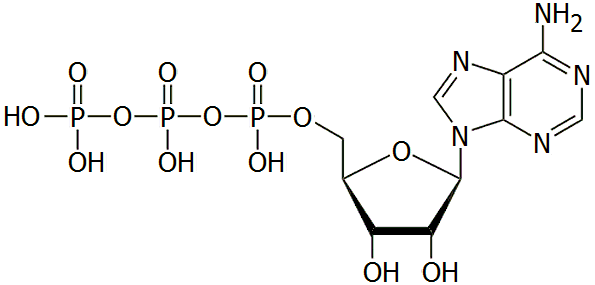
5'-Αδενοσινο-τριφωσφορικό οξύ (ATP)
5'-Adenosine-triphosphoric
acid (ATP)
|
|
 |
 |
|
Ο Γερμανός βιοχημικός
Hans Karl Heinrich Adolf Lohmann
(1898-1978). Δεξιά
χειρόγραφο του όπου διακρίνεται ο τύπος του ATP.
Το ότι δεν τιμήθηκε με βραβείο Nobel για την ανακάλυψη του τόσο
σημαντικού για τη βιοχημεία μορίου, αποτέλεσε θέμα πολλών
συζητήσεων. |
,
αλλά και στη μορφή εστέρων του διφωσφορικού (πυροφωσφορικού) οξέος (H4P2O7).
 |
 |
|
Αριστερά: ο Αμερικάνος
βιοχημικός
Cyrus H. Fiske (1890-1978). Δεξιά: ο Ινδός
Yellapragada SubbaRow (1895-1948). Οι δύο επιστήμονες του
Harvard οι οποίοι, ουσιαστικά συγχρόνως με τον Lohmann, ανακάλυψαν το ATP.
|
|
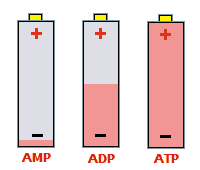
Τα μόρια του ATP συχνά παρομοιάζονται
ως επαναφορτιζόμενες μοριακές μπαταρίες. Ως 5'-αδενοσίνο-μονοφωσφορικό
οξύ (AMP) η μοριακή μπαταρία ουσιαστικά είναι "αφόρτιστη", ως
5'-αδενοσινο-διφωσφορικό οξύ (ADP) είναι κατά το ήμισυ φορτισμένη,
ενώ ως 5'-αδενοσινο-τριφωσφορικό οξύ (ATP) είναι πλήρως
φορτισμένο. |
|
 |
|
 |
 |
|
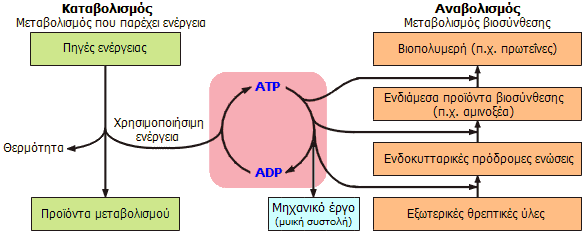
Συνοπτική παρουσίαση του μηχανισμού
φόρτισης/εκφόρτισης της "μοριακής μπαταρίας" του συστήματος
ATP/ADP:
Το ATP υδρολύεται προς
ADP και παρέχει την απαιτούμενη ενέργεια για τη βιοσύνθεση
των απαραίτητων βιομορίων για τη λειτουργία του κυττάρου και του
οργανισμού γενικότερα, δηλ. κατά τον αναβολισμό απλούστερων
ενώσεων σε πιο σύνθετα μόρια. Το ADP
επανασχηματίζει το ATP προσλαμβάνοντας
ενέργεια από την "καύση" των τροφών (σάκχαρα, λίπη, πρωτεΐνες), δηλ.
κατά τον καταβολισμό τους σε απλούστερα μόρια, μεγάλο μέρος
των οποίων χρησιμοποιείται κατά τον αναβολισμό. |
|
Αριστερά:
Fritz Albert Lipmann (1899-1986, Βραβείο Nobel Φυσιολογίας - Ιατρικής
του 1953). Δεξιά:
Herman
Kalckar (1908-1991). Ερμήνευσαν τον ρόλο του ATP
στις μεταβολικές διεργασίες στα κύτταρα και έθεσαν τις βάσεις
της βιοενεργητικής. |
|
 |
|
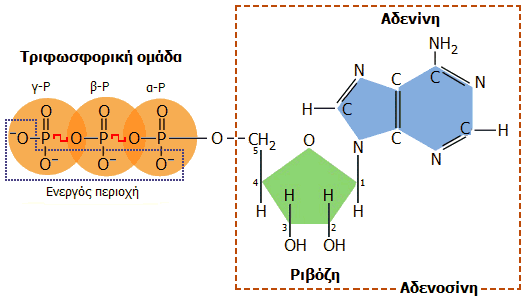
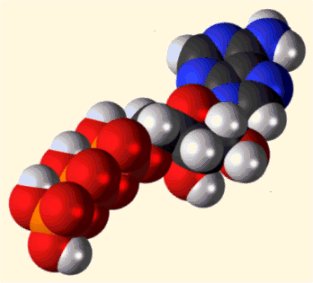
Συντακτικός τύπος (όπου διακρίνονται οι τρεις συστατικές μονάδες)
και τρισδιάστατη δομή του ATP. Η αποθηκευμένη ενέργεια βρίσκεται
στην τριφωσφορική ομάδα και ειδικότερα στους ομοιοπολικούς δεσμούς P-O που στο
σχήμα υποδεικνύονται με κόκκινο χρώμα. Η ενέργεια αυτή αποδίδεται κατά την
υδρόλυση των δεσμών αυτών. |
|
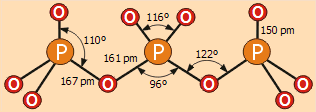
Δομή του
τριφωσφορικού ανιόντος P3O105- |
Πολυφωσφορικά οξέα και άλατα τους
[Αναφ. 3]
Ο φωσφόρος(V) εκτός από το κοινό
τριπρωτικό φωσφορικό οξύ (Η3PO4)
μπορεί να σχηματίσει μια σειρά πολυφωσφορικών οξέων με τον γενικό τύπο Η(n+2)
[PnO3n+1],
ως προϊόντα μερικής αφυδάτωσης του φωσφορικού οξέος. Η δομή τους έχει ένα κοινό
μοτίβο:
Τα τετράεδρα PO4
συνδέονται ανά δύο μεταξύ τους μέσω ενός κοινού ατόμου οξυγόνου. Τα πιο γνωστά από τα
οξέα αυτά είναι (με n = 2 και 3), δηλ. το διφωσφορικό οξύ (γνωστό και ως
πυροφωσφορικό οξύ) Η4P2O7
και το τριφωσφορικό οξύ H5P3O10,
ενώ έχουν απομονωθεί τα πολυφωσφορικά οξέα (ή άλατά τους) μέχρι n = 10. Εκτός
από τα γραμμικά πολυφωσφορικά οξέα είναι γνωστά και κυκλικά πολυφωσφορικά
οξέα, με γενικό τύπο Ηn[cyclo-(PO3)n]
(n = 3 - 8).
Πολυφωσφορικά οξέα με n από 10 έως 50
μπορούν να ληφθούν ως υαλώδη ή άμορφα μίγματα. Εξαντλητική αφυδάτωση (π.χ. n>50)
ουσιαστικά οδηγεί στο πολυμερούς χαρακτήρα
μεταφωσφορικό οξύ (ΗPO3)n.
2Η3PO4
 H4P2O7
+ H2O 3H3PO4 H4P2O7
+ H2O 3H3PO4
 H5P3O10
+ 2H2O
.... nH3PO4 H5P3O10
+ 2H2O
.... nH3PO4
 (HPO3)n + nH2O
(HPO3)n + nH2O
|
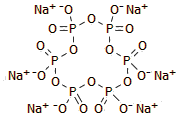
Κυκλοεξαμεταφωσφορικό νάτριο |
Πυροφωσφορικά άλατα παρασκευάζονται
εύκολα με θερμική συμπύκνωση μονόξινων ή δισόξινων φωσφορικών αλάτων, ενώ
τριφωσφορικά άλατα παρασκευάζονται σε βιομηχανική κλίμακα με ελεγχόμενη θέρμανση
μίγματος μονόξινου και δισόξινου φωσφορικού άλατος:
2NaH2PO4
 Na2H2P2O7 + H2O
2Na2HPO4
Na2H2P2O7 + H2O
2Na2HPO4
 Na4P2O7 + H2O 2Na2HPO4 + NaH2PO4
Na4P2O7 + H2O 2Na2HPO4 + NaH2PO4
 Na5P3O10 + 2H2O
Na5P3O10 + 2H2O
Τα υδατικά διαλύματα των αλάτων αυτών
υδρολύονται με αργό ρυθμό εκλύοντας θερμότητα, ταχύτερα δε σε όξινα διαλύματα.
'Aλατα του πυροφωσφορικού οξέος χρησιμοποιούνται ως
μαγειρικά πρόσθετα (όξινα και ουδέτερα άλατα) και ως λειαντικά υλικά σε
οδοντόπαστες. 'Aλατα του τριφωσφορικού οξέος χρησιμοποιήθηκαν ως πρόσθετα σε
συνθετικά απορρυπαντικά, λόγω της ικανότητάς τους να συμπλέκουν ισχυρά τα ιόντα
μαγνησίου και ασβεστίου, καθιστώντας τα ικανά να δράσουν ακόμη και
σε νερά υψηλής σκληρότητας.
Tο κυκλοεξαμεταφωσφορικό νάτριο, (NaPO3)6,
γνωστό και ως
άλας Graham (δεξιά), χρησιμοποιείται ως πρόσθετο τροφίμων (Ε452i) για την αύξηση
του pH, όπως επίσης και για την αποσκλήρυνση του ύδατος. |
Το
ATP ως οξύ και συμπλεκτικό αντίδραστήριο. Η
τριφωσφορική αλυσίδα καθιστά το
ATP ένα τετραπρωτικό οξύ. Και τα 4 υδροξύλια, που
είναι συνδεδεμένα με τα άτομα φωσφόρου (P-OH), μπορούν να υποστούν διάσταση.
Ωστόσο, η διάσταση του ATP
πέρα από το 2ο στάδιο προϋποθέτει αρκετά αλκαλικό διάλυμα που επιφέρει
ταχεία υδρόλυση της ένωσης. Σε σχετικώς πρόσφατη βιβλιογραφία αναφέρονται οι δύο πρώτες
σταθερές διάστασης: pKa1=
4,31
± 0,02 και
pKa2 = 6,76
± 0,02
(σε διάλυμα 0,10 Μ NaCl
στους 25ºC
[Αναφ. 1γ]).
Τα υδατικά διαλύματα του ATP
(ελαφρώς όξινα ως έχουν ή σε διάλυμα τριχλωροξικού οξέος) αναφέρονται ως σταθερά για λίγες ώρες στους 0ºC. Σταθερότερα
είναι τα διαλύματα του ATP σε ρυθμιστικά διαλύματα με
pH στην περιοχή 6,8-7,4. Ασταθέστατο είναι το ATP
σε αλκαλικά διαλύματα, όπου υδρολύεται ταχύτατα. Το
ATP φυλάσσεται καλύτερα στη μορφή άνυδρου άλατος
ή ως ένυδρο άλας σε κατάψυξη (-20ºC). Το ATP διατίθεται για ερευνητικούς
σκοπούς ως
διάλυμα 0,10 Μ το οποίο έχει ρυθμιστεί σε pH 7,0
με NaOH ή ως άλας με τρισυδροξυμεθυλαμινομεθάνιο
(γνωστό ως
Tris)
(C10H16N5O13P3·2C4H11NO3·2H2O)
[Αναφ.
4α,β].
Το ATP δρα και ως συμπλεκτικό αντιδραστήριο,
έχοντας την ικανότητα να συμπλέκει διάφορα μεταλλοϊόντα. Ιδιαίτερα σταθερό
είναι το σύμπλοκο με τα ιόντα Mg2+, τα οποία αποτελούν κανονικό
συστατικό του κυτταροπλάσματος. Η σύμπλεξη αυτή είναι επόμενο να τροποποιεί
τόσο τις σταθερές διάστασης, όσο και την υδρολυτική συμπεριφορά του ATP
καθιστώντας το σταθερότερο. Με
θερμομετρική ογκομέτρηση προσδιορίσθηκαν οι ακόλουθες τιμές της σταθεράς
σχηματισμού του ATP με τα αναφερόμενα ιόντα με τα οποία
σχηματίζει σύμπλοκα 1:1 [Αναφ. 4β-γ,
5β]:
Μg2+: 9554
±
585
Ca2+: 3722
±
211
Sr2+: 1381
±
120
Li+: 25 Na+:
13 K+: 8
Υδρόλυση του ATP.
Το 5'-αδενοσινο-τριφωσφορικό οξύ και τα δύο
παράγωγά του που προκύπτουν κατά τα διαδοχικά στάδια μερικής υδρόλυσής του,
το
5'-αδενοσινο-διφωσφορικό
οξύ (5'-adenosine
diphosphoric acid, ΑDP) και το
5'-αδενοσινο-μονοφωσφορικό
οξύ
(5'-adenosine monophosphoric
acid, ΑMP), δείχνονται παρακάτω:
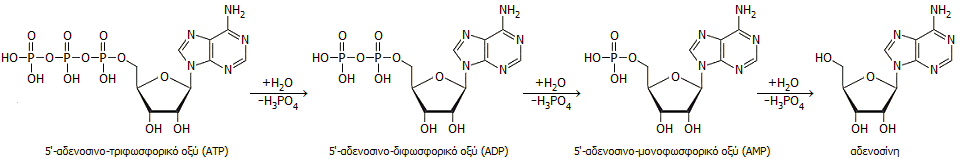
To ATP υδρολύεται εύκολα προς 5'-αδενοσινο-διφωσφορικό
οξύ (ADP) και
5'-αδενοσινο-μονοφωσφορικό οξύ (AMP) με έκλυση ενέργειας (εξεργονικές αντιδράσεις). Η ενέργεια αυτή εκλύεται ως
θερμότητα ή παρουσία κατάλληλου υποστρώματος (συζευγμένη αντίδραση) και ενζύμου μεταφέρεται ως χημική ενέργεια
μαζί με μια φωσφορική ομάδα στα τελικά προϊόντα της ενζυμικής αντίδρασης.
Η υδρόλυση του ATP προς AMP μπορεί να
πραγματοποιηθεί με δύο τρόπους: (α) Σταδιακά, όπως δείχνεται παραπάνω με
απελευθέρωση συνολικά 2 φωσφορικών οξέων (H3PO4).
(β) Απευθείας προς AMP με απελευθέρωση
διφωσφορικού
(ή πυροφωσφορικού) οξέος (H4P2O7)
το οποίο μπορεί να υδρολυθεί προς φωσφορικό οξύ. Οι σχετικές αντιδράσεις και
οι μεταβολές της ελεύθερης ενέργειας έχουν ως εξής
[Αναφ. 2ια]:
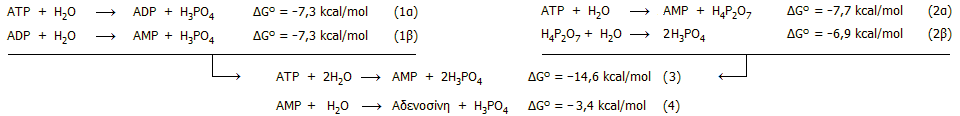
|

Alexander Todd
(1907-1997). Ο Σκώτος βιοχημικός που συνέθεσε πολλές ενώσεις
βιοχημικού ενδιαφέροντος. Ετιμήθηκε με το βραβείο
Nobel Χημείας το 1957. |
Από τις παραπάνω αντιδράσεις φαίνεται πως η
πλήρης υδρόλυση του ATP προς
AMP και φωσφορικό οξύ μπορεί να πραγματοποιηθεί
μέσω των δύο διαδρομών, δηλ. μέσω των αντιδράσεων
1α-1β ή μέσω των αντιδράσεων 2α-2β και προφανώς η συνολικά απελευθερούμενη
ενέργεια είναι η ίδια μέσω της μίας ή της άλλης διαδρομής. Ακόμη, από τις
τιμές ΔG είναι εμφανές ότι η ενέργεια των δύο
ακραίων δεσμών P-O (φωσφόροι γ-P
και β-P) είναι υπερδιπλάσια του αντίστοιχου δεσμού
P-O (φωσφόρου α-P) που
συνδέεται άμεσα με την αδενοσίνη. Στις περισσότερες περιπτώσεις βιοχημικών
αντιδράσεων τροφοδοτούμενων ενεργειακά από το ATP, αυτό υδρολύεται προς
ADP (αντίδραση 1α) και φωσφορικά ιόντα, ενώ σε λιγότερες το ATP υδρολύεται
απ' ευθείας προς AΜP και πυροφωσφορικά ιόντα (αντίδραση 2α).
Τα ηλεκτρόνια των φωσφορικών δεσμών έλκονται
προς διάφορες κατευθύνσεις και συγχρόνως απωθούνται από το αρνητικό φορτίο
των οξυγόνων που συνιστούν το φορτίο των ανιόντων του ATP. 'Ετσι βρίσκονται
σε μια "άβολη" υψηλή ενεργειακή κατάσταση. Κατά την υδρόλυση του
φωσφοανυδριτικού δεσμού
P-O-P τα ηλεκτρόνια των φωσφορικών ομάδων περιέρχονται σε μια πιο
"αναπαυτική" ενεργειακά χαμηλότερη θέση πλησιέστερα στους πυρήνες. Η διαφορά
των δύο ενεργειακών καταστάσεων είναι η εκλυόμενη κατά την υδρόλυση
ενέργεια.
Πρέπει να σημειωθεί ότι η αντίδραση εφυδάτωσης του P2O5
(υαλώδης μορφή)
προς H3PO4
παρέχει 29,1 kcal/mol ή 14,5
kcal για κάθε γραμμομόριο παραγόμενου Η3PΟ4. Το ποσόν αυτό της θερμότητας
συμβαδίζει με τα 7,3 kcal για κάθε γραμμομόριο
παραγόμενου Η3PΟ4, που παρέχει κάθε
(κατά
το ήμισυ εφυδατωμένος) φωσφόρος του
ATP κατά την "πλήρη εφυδάτωσή" του προς Η3PO4.
'Αλλες μορφές (άμορφο και κρυσταλλικό P2O5)
παρέχουν μεγαλύτερα ποσά θερμότητας (34-45 kcal/mol)
[Αναφ. 5α].
Οι παραπάνω αναφερόμενες τιμές ΔG
σε κάθε περίπτωση είναι πολύ υψηλές (συγκριτικά με εκείνες άλλων βιοχημικών
αντιδράσεων). Επιπλέον, πρέπει να θεωρηθούν ως ενδεικτικές, αφού αυτές εξαρτώνται σε κάποιο βαθμό από το περιβάλλον, π.χ.
από το pH και την παρουσία ιόντων που συμπλέκονται
με την τριφωσφορική ομάδα, όπως το Mg(II), όπως
προαναφέρθηκε. 'Εχουν
πραγματοποιηθεί διεξοδικές μελέτες πάνω στη θερμοδυναμική των
προηγούμενων αντιδράσεων. Βέβαια, βιοχημικό ενδιαφέρον έχουν οι τιμές οι
οποίες
λαμβάνονται σε συνθήκες παρόμοιες με εκείνες που επικρατούν στο
εσωτερικό των κυττάρων [Αναφ. 5β-γ].
Μεταφορά
της ελεύθερης ενέργειας του ATP σε μη αυθόρμητες αντιδράσεις. Η
αυθόρμητη διάσπαση του ATP προς ADP (ΔGº<0:
εξεργονική αντίδραση)
συζεύγνυται με αντίδραση, οι οποία δεν χωρεί
αυθόρμητα (ΔGº>0:
ενδεργονική αντίδραση).
Τυπικό παράδειγμα αποτελεί η αντίδραση φωσφορυλίωσης της γλυκερίνης:
Γλυκερίνη + φωσφορικό οξύ
 γλυκερινο-3-φωσφορικό οξύ, ΔG1º
= +2,2 kcal/mol.
γλυκερινο-3-φωσφορικό οξύ, ΔG1º
= +2,2 kcal/mol.
Η αντίδραση αυτή δεν
πραγματοποιείται αυθόρμητα. Ωστόσο, αν συζευχθεί με την αυθόρμητη διάσπαση του ATP:
ATP  ADP + φωσφορικό οξύ, ΔG2º
= -7,3 kcal/mol,
ADP + φωσφορικό οξύ, ΔG2º
= -7,3 kcal/mol,
η συνολική
αντίδραση γίνεται:
Γλυκερίνη + ATP
 γλυκερινο-3-φωσφορικό οξύ + ADP, ΔGολº
= ΔG1º
+ ΔG2º
= (+2,2 kcal/mol)
+ (-7,3 kcal/mol)
= -5,1 kcal/mol.
γλυκερινο-3-φωσφορικό οξύ + ADP, ΔGολº
= ΔG1º
+ ΔG2º
= (+2,2 kcal/mol)
+ (-7,3 kcal/mol)
= -5,1 kcal/mol.
Το αρνητικό πρόσημο του αθροίσματος των ελευθέρων ενεργειών δηλώνει ότι η
συνολική αντίδραση χωρεί αυθόρμητα (εξεργονικά) προς τα δεξιά. Συνολικά, το ATP
υπερκαλύπτει τις ενεργειακές ανάγκες της φωσφορυλίωσης της γλυκερίνης και το
περίσσευμα της ενέργειας που προσφέρει χάνεται ως θερμότητα. Το σύστημα των συζευγμένων αντιδράσεων
συνήθως παριστάνεται με καμπύλα βέλη όπως φαίνεται στο σχήμα κάτω αριστερά. Το
σχήμα περιγράφει δύο συζευγμένες αντιδράσεις, αλλά είναι δυνατόν να υπάρχει
μια αλληλουχία συζευγμένων αντιδράσεων, με κυκλική αναγέννηση των ενδιάμεσων
ουσιών (κάτω δεξιά). Θα πρέπει να τονισθεί ότι όλες οι αντιδράσεις χωρούν
παρουσία του αντίστοιχου για κάθε αντίδραση ενζύμου.

Σύνθεση του
5'-αδενοσινο-τριφωσφορικού
οξέος
Σύνθεση του
ATP στο εργαστήριο. Η
πρώτη εργαστηριακή σύνθεση του 5'-αδενοσινο-τριφωσφορικού οξέος πραγματοποιήθηκε από τον Σκώτο βιοχημικό
Alexander Todd
(1907-1997) και τους συνεργάτες του στο Πανεπιστήμιο του Cambridge
[Αναφ. 1θ, 6]. Η δυσκολία στη
συγκεκριμένη σύνθεση ήταν η εισαγωγή της τριφωσφορικής
ομάδας στην 5'-θέση της αδενοσίνης, της οποίας η σύνθεση είχε επιτευχθεί
παλαιότερα.
Χρησιμοποιήθηκε το αντιδραστήριο
χλωροφωσφoνικό διβενζύλιο, το οποίο παρασκευάζεται με χλωρίωση του
φωσφονικού (ή φωσφορώδους) διβενζυλεστέρα (dibenzyl phοsphonate, (C6H5CH2O)2P(=O)H), αντιδραστήριο το οποίο είχε ήδη χρησιμοποιηθεί για την εισαγωγή της διφωσφορικής
(πυροφωσφορικής) ομάδας.
Η αδενοσίνη αντιδρά με το χλωροφωσφονικό διβενζύλιο σε τρία
επιμέρους στάδια, στο καθένα από τα οποία εισάγεται μια φωσφορική ομάδα. Στη
συνέχεια οι βενζυλικές ομάδες απομακρύνονται με καταλυτική υδρογόνωσή τους
προς τολουόλιο (αποβενζυλίωση).
Αν και το συνθετικό σχήμα του Todd δείχνει απλό, παρουσιάζονται πρακτικές δυσκολίες
και ιδιαίτερα στο ενδιάμεσο στάδιο μερικής αποβενζυλίωσης του
τριβενζυλοπαραγώγου του διφωσφορικού (πυροφωσφορικού) εστέρα, όπου προσεκτικά πρέπει να
αποκαλυφθεί ένα μόνο υδροξύλιο, ώστε να προχωρήσει η σύνθεση στην εισαγωγή της
τρίτης σε σειρά φωσφορικής ομάδας. 'Αλλη σημαντική δυσκολία στη σύνθεση αποτελεί η
περιορισμένη σταθερότητα (λόγω εύκολης υδρόλυσης) του τελικού προϊόντος. Το γενικό σχήμα της σύνθεσης έχει ως εξής:
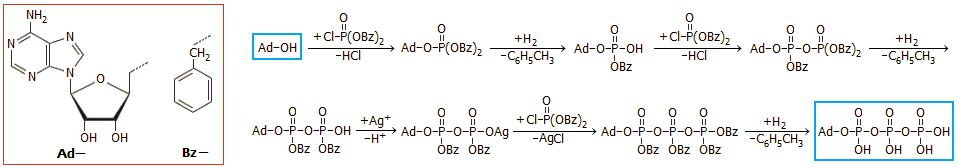
Αρχή της σύνθεσης του 5'-αδενοσινο-τριφωσφορικού
οξέος (ATP) που πραγματοποιήθηκε από τον Todd και τους συνεργάτες του (1948).
|
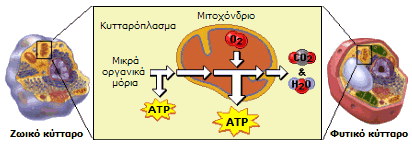
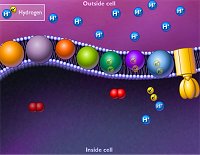
Το
ATP παράγεται στο κυτταρόπλασμα κατά
τον αναβολισμό μικρών οργανικών μορίων απουσία οξυγόνου, ωστόσο οι
μεγαλύτερες ποσότητές του παράγονται στα μιτοχόνδρια των κυττάρων
παρουσία οξυγόνου. |
Σύνθεση του ATP στους
ζώντες οργανισμούς. Η σύνθεση του ATP στους ζώντες οργανισμούς
πραγματοποιείται με δύο τελείως διαφορετικούς τύπους αντιδράσεων που προφανώς απαιτούν
την προσφορά ενέργειας:
(α) Σε επίπεδο υποστρώματος ενζυματικών
αντιδράσεων: μια φωσφορική ομάδα προστίθεται έμμεσα στο 5'-αδενοσίνο-διφωσφορικό
οξύ (ADP),
μέσω μιας ενδιάμεσης φωσφορυλιωμένης ένωσης. Ο κυριότερος τρόπος είναι η
γλυκόλυση, δηλ. η σταδιακή αποικοδόμηση της γλυκόζης προς πυροσταφυλικό
οξύ (2 μόρια ανά μόριο γλυκόζης). Η όλη διεργασία προσφέρει (καθαρά) 2 μόρια
ATP ανά 1 μόριο γλυκόζης, πραγματοποιείται στο κυτταρόπλασμα και δεν απαιτεί
οξυγόνο.
Στη συνέχεια το πυροσταφυλικό οξύ
μετατρέπεται σε ακετυλο-συνένζυμο, το οποίο εισέρχεται (ως "καύσιμο") στον κύκλο
Krebs, όπου παράγεται 1 μόριο ATP ανά μόριο εισερχόμενου πυροσταφυλικού
οξέος.
Η παραπάνω διεργασία πραγματοποιείται στα μιτοχόνδρια, τα οργανίδια του κυττάρου που έχουν χαρακτηρισθεί ως "εργοστάσια παραγωγής ενέργειας",
αν και ορθότερο θα ήταν να χαρακτηριστούν ως "εργοστάσια πακεταρίσματος ενέργειας", αφού η ενέργεια δεν "παράγεται", απλά υπάρχει και αλλάζει μορφές
("περιτύλιγμα"). Το συνολικό αποτέλεσμα
είναι μόνο 4 μόρια ATP ανά μόριο γλυκόζης.
Ωστόσο, κατά τα στάδια αυτά παράγεται
επιπλέον και σημαντικός αριθμός μορίων οξειδοαναγωγικών συνενζύμων (NADH και FADH2)
στην ενεργειακώς πλούσια ανηγμένη μορφή που θα αξιοποιηθούν στη συνέχεια.
(β) Οξειδωτική φωσφορυλίωση: Η διεργασία
αυτή είναι τελείως διαφορετική από την προηγούμενη, αν και πραγματοποιείται στον
ίδιο χώρο δηλ. στα μιτοχόνδρια. Κατά το στάδιο αυτό
το Ο2
γίνεται ο τελικός αποδέκτης των ηλεκτρονίων που μεταφέρουν
οι ανηγμένες μορφές των οξειδοαναγωγικών συνενζύμων που συμπαρήχθησαν μαζί με το ATP στις προηγούμενες διεργασίες.
Η ενέργεια που εκλύεται δεσμεύεται σε επιπλέον 32 μόρια ATP.
Με βάση τα προηγούμενα, από την "καύση" 1 μορίου
γλυκόζης παράγονται συνολικά 36 μόρια ATP. Περισσότερες λεπτομέρειες
πάνω στα διάφορα στάδια του καταβολισμού της γλυκόζης, του κύκλου Krebs και των
εκπληκτικών μηχανισμών που συνιστούν την οξειδωτική φωσφορυλίωση, όπως
και του παράδοξου ως προς τον τρόπο λειτουργίας του ενζύμου-"μοριακής μηχανής",
το οποίο βιοσυνθέτει το ATP παρουσιάζονται στη συνέχεια.
Βασικά στοιχεία
μεταβολισμού
|
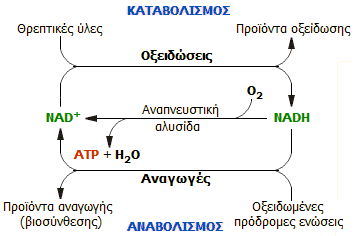
Γενική διάκριση
μεταβολικών διεργασιών σε καταβολικές και αναβολικές |
Ως
μεταβολισμός
(metabolism) ορίζεται το σύνολο των χημικών
μετασχηματισμών οι οποίοι πραγματοποιούνται μέσα στα κύτταρα των ζώντων
οργανισμών. Οι αντιδράσεις αυτές καταλύονται από ένζυμα και καθιστούν τους
ζώντες οργανισμούς ικανούς να αναπτυχθούν, να συντηρηθούν, να αναπαραχθούν, να αποκριθούν και να
προσαρμοστούν στο περιβάλλον τους. Ως μεταβολισμός αναφέρεται και το σύνολο των
χημικών αντιδράσεων που πραγματοποιούνται στους ζώντες οργανισμούς, στις οποίες
περιλαμβάνονται οι διαδικασίες χώνευσης και μεταφοράς των ουσιών μεταξύ των
διαφόρων κυττάρων.
Το σύνολο των αντιδράσεων του μεταβολισμού
χωρίζονται σε δύο κατηγορίες:
(α) Αντιδράσεις καταβολισμού. Κατά τις
αντιδράσεις αυτές θρεπτικές οργανικές ουσίες που λαμβάνονται ως τροφή, ή βρίσκονται αποθηκευμένες στον ζώντα οργανισμό, διασπώνται με σκοπό την παραγωγή ενέργειας,
όπως και τον σχηματισμό απλούστερων ενώσεων οι οποίες θα χρησιμοποιηθούν ως δομικά στοιχεία για
τη σύνθεση ουσιών απαραίτητων για τη διατήρηση της ζωής. Μέρος των
σχηματιζόμενων απλούστερων ενώσεων
αποβάλλεται ως άχρηστο ή τοξικό για τον οργανισμό.
(β) Αντιδράσεις
αναβολισμού. Κατά τις αντιδράσεις αυτές χρησιμοποιούνται η ενέργεια και οι απλούστερες
ενώσεις (δομικά στοιχεία), που ελήφθησαν κατά τον καταβολισμό, για τη σύνθεση πολυπλοκότερων ενώσεων απαραίτητων για την ανάπτυξη και διατήρηση
του ζώντος οργανισμού.
|
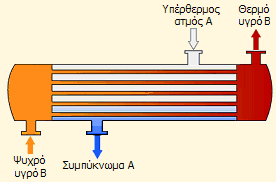
Βιομηχανικός
εναλλάκτης θερμότητας. Με τους εναλλάκτες
θερμότητας αξιοποιείται η θερμική ενέργεια που εκλύεται σε κάποιο
στάδιο της βιομηχανικής παραγωγής, αντί να αφεθεί να διαχυθεί στο
περιβάλλον. |
Διακίνηση ενέργειας.
Σε μια σωστά σχεδιασμένη βιομηχανική μονάδα χημικής σύνθεσης, όταν σε κάποιο στάδιο της όλης διεργασίας
εκλύεται θερμότητα, λόγοι ενεργειακής οικονομίας επιβάλλουν η
θερμότητα αυτή να μη χαθεί διαχεόμενη στο περιβάλλον, αλλά κατά το δυνατόν να αξιοποιηθεί
π.χ. για τη θέρμανση άλλων χημικών αντιδραστήρων, όπου απαιτείται θέρμανση για
να πραγματοποιηθούν κάποιες άλλες αντιδράσεις. Αυτό πραγματοποιείται με τους
λεγόμενους εναλλάκτες θερμότητας (heat exchangers),
όπου ένα θερμό αέριο ή υγρό (συνήθως υπέρθερμος ατμός), κυκλοφορεί μέσω σωλήνων
που βρίσκονται σε επαφή με ένα άλλο σύστημα σωληνώσεων, όπου κυκλοφορεί ένα άλλο
ρευστό, το οποίο παραλαμβάνει ποσά θερμότητας από το προηγούμενο.
Στους ζωντανούς οργανισμούς δεν μπορεί να συμβεί κάτι
αντίστοιχο. Στους οργανισμούς μεγάλο μέρος της εκλυόμενης ενέργειας από τις
βιοχημικές αντιδράσεις καταβολισμού (που συχνά αναφέρονται ως "καύσεις" του οργανισμού) αποθηκεύεται
προσωρινά σε βιοχημικές ενώσεις υψηλής ενέργειας με κυριότερο αλλά και
"σταθερότερο" εκπρόσωπό τους το ATP. 'Ετσι, αυτές οι
αντιδράσεις συζεύγνυνται άμεσα ή έμμεσα με την αντίδραση φωσφορυλίωσης μορίων
ADP προς ATP.
Στη συνέχεια,
τα μόρια
ATP, δρώντας ως συνένζυμο, συζεύγνυνται με ενζυμικές
αντιδράσεις προσφέροντας την εκάστοτε απαιτούμενη ενέργεια. Οι αντιδράσεις αυτές
είναι κατά κανόνα αντιδράσεις φωσφορυλίωσης απλών οργανικών μορίων προϊόντων καταβολικών
(κυρίως) διεργασιών. Στις συνθήκες που επικρατούν στο κύτταρο, το ATP δεν μπορεί μόνο
του (δηλ. απουσία ενζύμου) να
υδρολυθεί και να απαλλαγεί από το ενεργειακό περιεχόμενό του, κάτι που αν συνέβαινε
θα το καθιστούσε άχρηστο από βιοχημική άποψη.
Κλασικός είναι ο χαρακτηρισμός του ATP ως "ενεργειακής νομισματικής μονάδας" και έτσι
υπεισέρχεται σε υπολογισμούς του "ενεργειακού ισοζυγίου" και
σε ενεργειακές "κοστολογήσεις" βιοχημικών διεργασιών. Για παράδειγμα, συχνά αναφέρεται ότι "η Α καταβολική αλληλουχία αντιδράσεων αποδίδει τόσες μονάδες (μόρια) ATP
ανά μόριο διασπώμενης ουσίας" ή,
ανάλογα, "η Β αναβολική αλληλουχία αντιδράσεων απαιτεί τόσες μονάδες (μόρια) ATP
ανά μόριο σχηματιζόμενης ουσίας".
Για να χαρακτηρισθεί μια βιοχημική ένωση ως ένωση
υψηλής ενέργειας θα πρέπει η ελεύθερη ενέργεια υδρόλυσής της να ξεπερνά τα 7 kcal/mol. Κατά κανόνα βιοχημικές ενώσεις υψηλής
ενέργειας είναι παράγωγα του φωσφορικού οξέος. Τυπικά παραδείγματα είναι οι
ανάλογες με την ΑΤP και ΑDP
ενώσεις με άλλες
πουρινικές και
πυριμιδινικές βάσεις (ουρακίλη,
θυμίδινη,
κυτοσίνη,
γουανίνη,
ινοσίνη,
οι οποίες συμβολίζονται αντίστοιχα ως UTP, UDP, TTP, TDP, CTP, CDP, GTP,
GDP, ITP και IDP), αλλά και
πολλές άλλες ενώσεις, όπως οι επόμενες
[Αναφ. 2ια]:
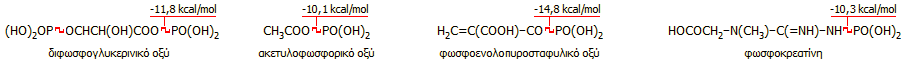
Διακίνηση ηλεκτρονίων.
Το "αρχικό" οξειδωτικό μέσον που χρησιμοποιούν όλοι οι
αερόβιοι οργανισμοί στις οξειδωτικές καταβολικές αντιδράσεις είναι το ατμοσφαιρικό οξυγόνο το οποίο προσλαμβάνεται με την
αναπνοή. Από τις αντιδράσεις αυτές αντλούν ενέργεια, όπως και τις πρόδρομες
ενώσεις για τις αναβολικές συνθέσεις. Ωστόσο, το ίδιο το οξυγόνο δεν μπορεί να είναι διαθέσιμο σε κάθε
σημείο όπου θα πρέπει να πραγματοποιηθεί μια οξείδωση, ούτε αποτελεί
την κατάλληλη μορφή οξειδωτικού για να προχωρήσουν οι καταβολικές αντιδράσεις με την
απαιτούμενη εκλεκτικότητα και ταχύτητα.
Οι οργανισμοί διαθέτουν πλήθος ουσιών σχετικά μικρού μοριακού βάρους,
οι οποίες δρουν ως συνένζυμα και υφίστανται τόσο σε οξειδωμένη, όσο και σε ανηγμένη μορφή. Πρόκειται για οξειδοαναγωγικά
ζεύγη που χαρακτηρίζονται από εξαιρετική ηλεκτροχημική αντιστρεπτότητα και των
οποίων η ανηγμένη τους μορφή δρα ως φορέας αναγωγικής ισχύος (δότες ηλεκτρονίων). Συχνά, τα ζεύγη
αυτά αναφέρονται ως "διακινητές
ηλεκτρονίων" ή -ισοδύναμα- ως "διακινητές ατόμων υδρογόνου". Οι ουσίες
αυτές δρουν σε πλήρη συνεργασία με τις ενώσεις υψηλής
ενέργειας, οι οποίες δρουν ως διακινητές ενέργειας, ωστόσο και οι ίδιες στην ανηγμένη μορφή
τους είναι ενεργειακώς πλούσιες
και την ενέργεια αυτή την αποδίδουν κατά την οξείδωσή τους.
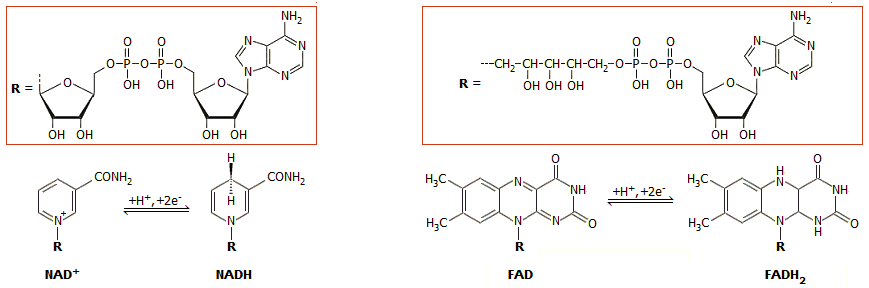
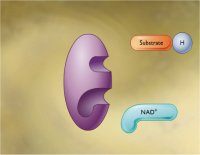
Ο πλέον τυπικός εκπρόσωπος των ενώσεων αυτών είναι το
νικοτιναμιδο-αδενινο-δινουκλεοτίδιο
(nicotinamide adenine dinucleotide,
NAD+/NADH), το οποίο συμβολίζεται στην οξειδωμένη (ή
οξειδωτική) μορφή ως NAD+ (το + δηλώνει
θετικό φορτίο εντοπισμένο στο νικοτιναμίδιο και όχι ότι η οξειδωμένη μορφή έχει
συνολικό φορτίο +1) και στην ανηγμένη (ή αναγωγική) μορφή ως NADH. Κατά τις
καταβολικές αντιδράσεις η οξειδωμένη μορφή δρα ως οξειδωτικό, παραλαμβάνοντας
ηλεκτρόνια από την οξειδούμενη ουσία. Κατά τις αναβολικές αντιδράσεις η ανηγμένη μορφή
NADH δρα ως
φορέας ηλεκτρονίων και προσφέρει την απαραίτητη αναγωγική ισχύ.
Ο γραμμομοριακός λόγος των ελεύθερων μορφών NAD+/NADH
στο κυτταρόπλασμα καθορίζει τη λεγόμενη οξειδοαναγωγική κατάσταση του
κυττάρου και κυμαίνεται γύρω από την τιμή 700 στα υγιή κύτταρα των θηλαστικών,
ενώ ο λόγος των συνολικών συγκεντρώσεών τους (ελεύθερα + δεσμευμένα σε πρωτεΐνες)
κυμαίνεται από 3 έως 10. Η ανηγμένη μορφή του συνενζύμου (NADH) είναι ισχυρό
αναγωγικό σώμα και ο σχηματισμός της από τη μορφή NAD+ απαιτεί
προσφορά χημικής ενέργειας, που λαμβάνεται από το ATP ή άλλες ενεργειακώς
πλούσιες ενώσεις.
'Αλλα ανάλογα συνένζυμα - οξειδοαναγωγικά ζεύγη είναι εκείνα του
φλαβινο-αδενινο-δινουκλεοτίδιο (flavino
adenino dinucleotide, FAD/FADH2)
και του
νικοτιναμιδο-αδενινο-φωσφορικού δινουκλεοτιδίου (nicotinamide
adenine dinucleotide phosphate, NADP+/NADPH),
ενός φωσφορυλιωμένου (στη ριβόζη) παραγώγου του NAD+/NADH.
'Αλλοι τελείως διαφορετικοί
τύποι ενώσεων διακινητών ηλεκτρονίων είναι διάφορα πεπτίδια με θειούχα αμινοξέα
(π.χ. γλουταθείον), κινοειδούς χαρακτήρα ενώσεις (π.χ. ουβικινόνη), βιταμίνες
(π.χ. ασκορβικό οξύ), σιδηρο-θειο-πρωτεΐνες κ.α.
Γενικό σχήμα διάμεσου μεταβολισμού. Κατά
τις διαδικασίες του μεταβολισμού πραγματοποιείται τεράστιος αριθμός
βιοχημικών αντιδράσεων, κάθε μία από τις οποίες καταλύεται από ένα
εξειδικευμένο ένζυμο. Οι περισσότερες από τις αντιδράσεις αυτές
είναι συζευγμένες με αντιδράσεις, στις οποίες συμμετέχουν συνένζυμα
διακίνησης ενέργειας, όπως το ATP, όπως και συνένζυμα
διακίνησης ηλεκτρονίων, εφόσον πρόκειται για αντιδράσεις οξείδωσης ή
αναγωγής. Το γενικό σχήμα του διάμεσου μεταβολισμού δείχνεται στο επόμενο
σχήμα:
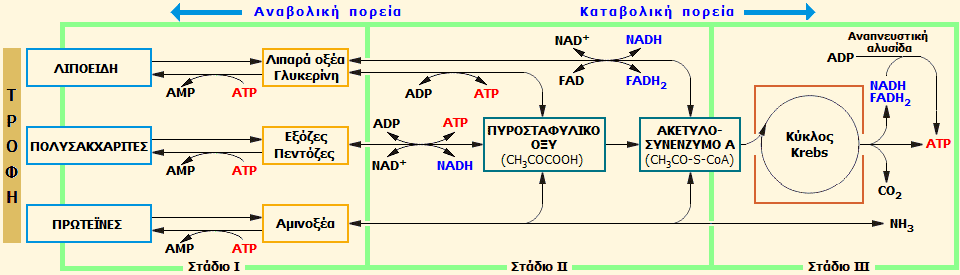
Τα τρία στάδια του διάμεσου
μεταβολισμού (με βάση την [Αναφ. 2ια], σχήμα 293).
Στο γενικό σχήμα του διάμεσου καταβολισμού διακρίνονται τρία
στάδια Ι, ΙΙ και ΙΙΙ. Ο καταβολισμός ακολουθεί την πορεία είναι Ι
 ΙΙ
ΙΙ
 ΙΙΙ και ο
αναβολισμός την αντίθετη ΙΙΙ
ΙΙΙ και ο
αναβολισμός την αντίθετη ΙΙΙ
 ΙΙ
ΙΙ
 Ι. Τα
χαρακτηριστικά γνωρίσματα κάθε σταδίου και κατά πορεία συνοψίζονται στον
ακόλουθο πίνακα:
Ι. Τα
χαρακτηριστικά γνωρίσματα κάθε σταδίου και κατά πορεία συνοψίζονται στον
ακόλουθο πίνακα:
|
Στάδιο |
Κοινά χαρακτηριστικά |
Καταβολική
πορεία |
Αναβολική
πορεία |
|
Ι |
Μη αμφίδρομες ενζυμικές αντιδράσεις - Δεν υπάρχουν οξειδοαναγωγικές
αντιδράσεις |
Εξεργονικές
αντιδράσεις (ΔG<0) - Η εκλυόμενη
ενέργεια δεν δεσμεύεται ως χημική (π.χ. με σχηματισμό
ATP) |
Ενδεργονικές
αντιδράσεις (ΔG>0)
- Η ενέργεια παραλαμβάνεται από το ATP -
Το ATP
υδρολύεται προς AMP |
|
ΙΙ |
- Αμφίδρομες ενζυμικές αντιδράσεις
-
Το ATP
μεταφέρει ενέργεια από εξεργονικές σε ενδεργονικές αντιδράσεις - Υπάρχουν οξειδοαναγωγικές αντιδράσεις
καταλυόμενες από τα συνένζυμα/διακινητές ηλεκτρονίων |
Αποδίδεται το 1/3 της ελεύθερης
ενέργειας κατά την καύση των μονομερών - Μέρος της εκλυόμενης
ενέργειας δεσμεύεται στο παραγόμενο ATP |
Δεσμεύεται το 1/3 της ελεύθερης
ενέργειας για τη σύνθεση των μονομερών από τις διαθέσιμες ποσότητες
ATP |
|
ΙΙΙ |
- Κοινό στάδιο και για τις τρεις τάξεις
θρεπτικών ουσιών - 'Ολες τους έχουν καταλήξει στη μορφή του "κοινού καυσίμου",
το ακετυλο-συνένζυμο
Α (CH3CO-S-CoA) που τροφοδοτεί τον κύκλο του Krebs - Χαρακτηρίζει
αποκλειστικά αερόβιους οργανισμούς - Πλήρης καύση στα μιτοχόνδρια
(τελικά προϊόντα: H2O,
CO2,
NH3
ή παράγωγά της, όπως η ουρία και το ουρικό οξύ) - Απόδοση των υπολοίπων 2/3 της ελεύθερης ενέργειας
των αρχικών μονομερών |
Γλυκόλυση [Αναφ.
7]
Η γλυκόζη θεωρείται ως η θρεπτική ύλη -
"καύσιμο άμεσης δράσης". Κατά
κανόνα, ο καταβολισμός της γλυκόζης αποτελεί τo κλασικότερo παράδειγμα
υπολογισμού του
"ενεργειακού ισοζυγίου", το οποίο εκφράζεται
σε μόρια ATP που μπορούν να
παραχθούν από την "καύση" ενός μορίου γλυκόζης.
Η αντίδραση πλήρους
και άμεσης και πλήρους καύσης της γλυκόζης από το οξυγόνο έχει ως εξής:
C6H12O6
+ 6 O2
 6 CO2 + 6 H2O, ΔGo
= -686 kcal/mol
6 CO2 + 6 H2O, ΔGo
= -686 kcal/mol
Από την τιμή
της μεταβολής της ελεύθερης ενέργειας της πλήρους καύσης θα περίμενε
κανείς ότι η πλήρης καύση 1 μορίου γλυκόζης θα μπορούσε να μετατρέψει 686/7,3 = 94
μόρια ADP σε ATP, ωστόσο αυτό δεν ισχύει διότι η γλυκόζη δεν "καίγεται" ποσοτικά σύμφωνα με την παραπάνω εξίσωση.
Πολλά από τα ενδιάμεσα προϊόντα της "καύσης" της χρησιμοποιούνται ως πρώτες ύλες για τον
αναβολισμό (σύνθεση πρωτεϊνών, λιποειδών, γλυκογόνου), κυρίως όμως, μεγάλο μέρος της
ενέργειας μετατρέπεται σε θερμότητα, που διατηρεί σταθερή τη θερμοκρασία του
οργανισμού (θερμόσταση) σε τιμή η οποία εξασφαλίζει μια εναρμονισμένη
ταχύτητα των βιοχημικών αντιδράσεων. Το ίδιο ισχύει και για τις άλλες θρεπτικές ύλες όπως τα
λιποειδή και τις πρωτεΐνες. Καμία θρεπτική ύλη δεν καίγεται πλήρως.
Η κατά στάδια οξείδωση της
γλυκόζης παρέχει την ενέργειά της στον ζώντα οργανισμό βαθμιαία και κατά
ελεγχόμενο τρόπο και όχι εκρηκτικά, όπως π.χ. θα συνέβαινε κατά την άμεση οξείδωσή της από το
οξυγόνο σε μια "βόμβα οξυγόνου" ενός
θερμιδομέτρου.
Ο καταβολισμός της γλυκόζης ξεκινά στο κυτταρόπλασμα
χωρίς την άμεση χρήση του οξυγόνου ως οξειδωτικού μέσου. Η διαδικασία αυτή
είναι γνωστή ως γλυκόλυση. Το τελικό προϊόν της γλυκόλυσης είναι το πυροσταφυλικό
οξύ (pyruvic acid) και δύο μόρια ATP (ως καθαρό "ισοζύγιο"
καταναλισκόμενων - παραγόμενων μορίων ATP). Η αλυσίδα των αντιδράσεων,
η καθεμία από τις οποίες καταλύεται από συγκεκριμένο ένζυμο, έχει ως εξής:
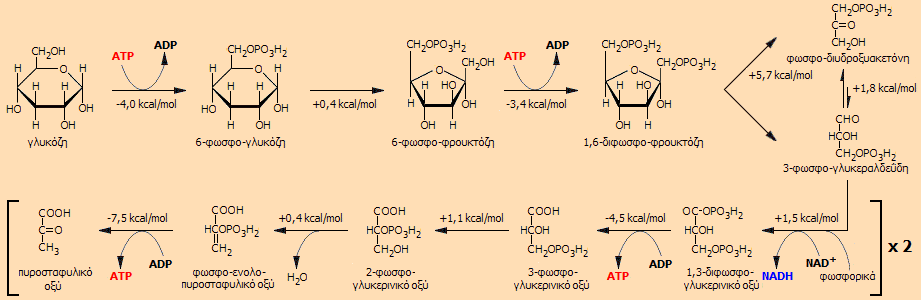
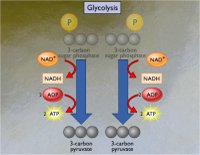
Αλληλουχία αντιδράσεων
γλυκόλυσης. Για κάθε βήμα δίνεται η μεταβολή της ελεύθερης ενέργειας ΔGo
[Αναφ.
7].
Η γλυκόλυση αρχίζει με μια
"επένδυση" προϋπάρχοντος ATP: με την άμεση
αντίδραση γλυκόζης - ATP.
Το ATP παρέχει την ενέργειά του και μια φωσφορική ομάδα σχηματίζοντας 6-φωσφο-γλυκόζη, η
οποία ισομερίζεται προς 6-φωσφο-φρουκτόζη. Η 6-φωσφο-φρουκτόζη
αντιδρά με ένα δεύτερο μόριο ATP και δέχεται μια επιπλέον φωσφορική ομάδα,
όπως και επιπλέον
ενέργεια παρέχοντας την υψηλής ενέργειας ένωση
1,6-διφωσφο-φρουκτόζη.
Η 1,6-διφωσφο-φρουκτόζη είναι ένωση με μεγάλο
ενεργειακό περιεχόμενο, γεγονός το οποίο προκαλεί την αυτοδιάσπασή της.
Πράγματι, ένας από τους δεσμούς C-C διασπάται παρέχοντας δύο φωσφορυλιωμένες τριόζες,
την 3-φωσφο-διυδροξυακετόνη και την 3-φωσφο-γλυκεραλδεΰδη,
οι οποίες βρίσκονται μεταξύ τους σε ισορροπία. Ολόκληρη η ποσότητα της
3-φωσφο-διυδροξυακετόνης μεταπίπτει σε 3-φωσφο-γλυκεραλδεΰδη, αφού η τελευταία απομακρύνεται
οξειδούμενη στο επόμενο ενδιάμεσο, το 1,3-διφωσφο-γλυκερινικό οξύ.
Το στάδιο της οξείδωσης της 3-φωσφο-γλυκεραλδεΰδης από το
NAD+ αποτελεί το κυριότερο σημείο
συλλογής ενέργειας. Κατά το στάδιο αυτό αποθηκεύεται ενέργεια
(ως "αναγωγική ενέργεια" ή ως "διαθέσιμο
υδρογόνο") αφενός μεν στο NADH, αφετέρου στο
1,3-διφωσφογλυκερινικό οξύ, ένωση υψηλής ενέργειας.
Αξιοσημείωτο είναι το ότι η φωσφορυλίωση πραγματοποιείται από ανόργανα φωσφορικά ιόντα
χωρίς κατανάλωση ATP. Την ενέργεια αυτή την
αποδίδει κατά τη μερική αποφωσφορυλίωσή του προς 3-φωσφογλυκερινικό οξύ
με φωσφορυλίωση ADP προς ATP.
Το 3-φωσφο-γλυκερινικό οξύ ισομερίζεται προς
2-φωσφο-γλυκερινικό οξύ, το οποίο αφυδατώνεται προς φωσφο-ενολο-πυροσταφυλικό
οξύ. Η τελευταία είναι ένωση υψηλής ενέργειας την οποία αποδίδει με φωσφορυλίωση
επιπλέον ADP προς
ATP παρέχοντας το τελικό προϊόν αυτού του κύκλου
το οποίο είναι το
πυροσταφυλικό οξύ. Συνοπτικά η συνολική
αντίδραση μπορεί να αποδοθεί ως εξής (τα μόρια ύδατος παραλείπονται):
γλυκόζη
+ 2 NAD+ + 2 φωσφορικά + 2 ADP
 2
πυροσταφυλικό οξύ (CH3COCOOH) + 2 NADH + 2
ATP + 2 H+ + θερμότητα
(1)
2
πυροσταφυλικό οξύ (CH3COCOOH) + 2 NADH + 2
ATP + 2 H+ + θερμότητα
(1)
Η παραπάνω συνολική αντίδραση δηλώνει ότι ένα μόριο
γλυκόζης κατά τη γλυκόλυση αποδίδει χημική ενέργεια σχηματίζοντας 2 μόνο μόρια
ATP, 2 μόρια
NADH (αποθήκευση αναγωγικής ισχύος), δύο μόρια πυροσταφυλικού οξέος και θερμότητα.
Η ίδια διαδικασία, κάτω από αναερόβιες συνθήκες
(σε ζυμώσεις) ή σε ορισμένους μικροοργανισμούς, αντί πυροσταφυλικού οξέος θα
δώσει την ανηγμένη μορφή του, το γαλακτικό οξύ
(γαλακτική ζύμωση) ή αιθανόλη + CO2 (αλκοολική ζύμωση).
Ανάλογες αλληλουχίες παρέχουν και άλλα σάκχαρα μονομερή ή σάκχαρα πολυμερή (δισακχαρίτες,
πολυσακχαρίτες) μετά από την υδρόλυσή τους.
Κύκλος
Krebs [Αναφ. 9]
Ακετυλίωση συνενζύμου Α. H ακετυλίωση του συνενζύμου Α αποτελεί το προκαταρκτικό στάδιο
το οποίο
συνδέει το στάδιο της γλυκόλυσης με το επόμενο στάδιο, που είναι ο κύκλος
του Krebs. Στο σημείο αυτό συναντώνται οι
καταβολικές πορείες υδατανθράκων, λιπών και πρωτεϊνών. To πυροσταφυλικό οξύ
επέχει κεντρικό-μεσολαβητικό ρόλο στον μεταβολισμό, αφού αποτελεί το κοινό προϊόν του καταβολισμού
κάθε είδους θρεπτικής ύλης και από αυτό ξεκινάει ο αναβολισμός κάθε
απαραίτητης ύλης για τον οργανισμό. Στο στάδιο
αυτό, το πυροσταφυλικό οξύ από το
κυτταρόπλασμα θα εισέλθει στα μιτοχόνδρια, όπου θα συμβεί η ακόλουθη
αντίδραση οξείδωσης:
πυροσταφυλικό οξύ (CH3COCOOH)
+ NAD+ + συνένζυμο Α (HS-CoA)
 ακετυλο-συνένζυμο Α (CH3CO-S-CoA) +
NADH + CO2
(2)
ακετυλο-συνένζυμο Α (CH3CO-S-CoA) +
NADH + CO2
(2)
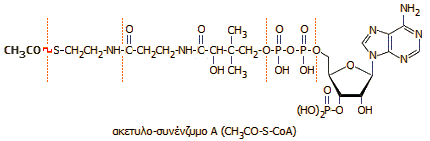
Το
πυροσταφυλικό οξύ αντιδρά με το
συνένζυμο
Α (coenzyme A), μια ένωση
κυστεαμίνης -
παντοθενικού
οξέος (βιταμίνη Β5)
- πυροφωσφορικού οξέος - φωσφορυλιωμένης αδενοσίνης, η οποία διαθέτει μια ελεύθερη θειολική ομάδα (-SH)
στην "ουρά" του κυστεαμίνης. Το συνένζυμο Α είναι το βασικό
μόριο-"μεταφορέας".
Το πυροσταφυλικό οξύ
ακετυλιώνει το συνένζυμο Α στη θειολική ομάδα παρέχοντας το
ακετυλο-συνένζυμο Α
(CH3CO-S-CoA)
και
CO2, ενώ συγχρόνως ανάγει ένα μόριο NΑD+
προς NADH.
Το ακετυλο-συνένζυμο Α εισέρχεται στον
κύκλο Krebs και τον τροφοδοτεί ενεργειακά μέσω του πλούσιου
σε ενέργεια δεσμού -C(=Ο)-S-. Εκεί θα οξειδωθεί
πλήρως το ακετύλιό του και θα επανασχηματισθεί το
συνένζυμο Α, το οποίο δρώντας ως "μεταφορέας", θα φέρει ένα νέο ακετύλιο
στον κύκλο Krebs.
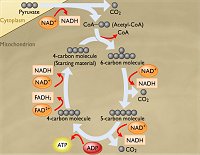
Κύκλος
Krebs.
O
κύκλος Krebs , γνωστός
και ως κύκλος κιτρικού οξέος ή κύκλος τρικαρβοξυλικού οξέος (tricarboxylic acid cycle, TCA),
είναι ο σημαντικότερος και διασημότερος βιοχημικός κύκλος. Κάθε βιοχημικός
κύκλος αποτελείται από μια αλληλουχία αντιδράσεων που ξεκινάει από μία ένωση
και καταλήγει στην ίδια. Ο κύκλος του Krebs ξεκινάει με το οξαλοξικό οξύ, τροφοδοτείται με ακετυλοσυνένζυμο Α και με μια αλυσίδα
αντιδράσεων, που πραγματοποιούνται στα μιτοχόνδρια των κυττάρων όλων των
αερόβιων οργανισμών, μετασχηματίζει την ενέργεια ολοκληρωτικής
οξείδωσης του ακετυλίου σε
ATP, αλλά και στις αναγωγικές μορφές των οξειδοαναγωγικών
συνενζύμων (NADH και
FADH2).
Επιπλέον, παρέχει πρόδρομες
ενώσεις για τη βιοσύνθεση αμινοξέων και από αυτά των πρωτεϊνών.
Αυτός ο διάσημος και εκπληκτικός βιοχημικός κύκλος προτάθηκε
το 1937 από τον Βρετανό (Γερμανικής καταγωγής) ιατρό και βιοχημικό
Hans
Adolf Krebs (1900-1980) του Πανεπιστημίου του
Sheffield, o οποίος τιμήθηκε για την ανακάλυψη αυτή
με το βραβείο Nobel Ιατρικής και Φυσιολογίας το
1953
Ο κύκλος του
Krebs αποτελεί το κοινό στάδιο ΙΙΙ οξείδωσης όλων των θρεπτικών υλών
που έχουν μετατραπεί σε ακετυλο-συνένζυμο Α, όπως αναφέρθηκε προηγουμένως. Περιγράφεται από το ακόλουθο συνοπτικό κυκλικό σχήμα βιοχημικών
αντιδράσεων, καθεμία από τις οποίες καταλύεται από συγκεκριμένο ένζυμο:
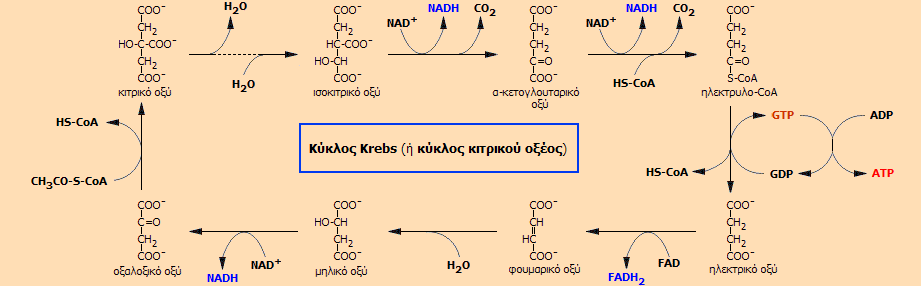
O
κύκλος Krebs , γνωστός
και ως κύκλος κιτρικού οξέος ή κύκλος τρικαρβοξυλικού οξέος (tricarboxylic acid cycle, TCA)
Σύμφωνα με τα προηγούμενα,
για κάθε ένα μόριο γλυκόζης παράγονται δύο μόρια
CH3CO-S-CoA και επομένως πραγματοποιούνται δύο κύκλοι.
Σε κάθε κύκλο οι δύο άνθρακες του ακετυλίου οξειδώνονται προς
CO2
το οποίο αποβάλλεται από την οργανισμό με την εκπνοή, ωστόσο χωρίς ακόμη να
χρησιμοποιηθεί άμεσα ως οξειδωτικό το Ο2.
Η συνολική αντίδραση που
περιγράφει ο κύκλος Krebs είναι η ακόλουθη (τα μόρια ύδατος παραλείπονται):
ακετυλο-συνένζυμο Α (CH3CO-S-CoA) + 3 NAD+ + FAD + ADP + φωσφορικά  3 NADH + FADH2 + ATP + 2
CO2 + 2 H+ + συνένζυμο Α (ΗS-CoA) (3)
3 NADH + FADH2 + ATP + 2
CO2 + 2 H+ + συνένζυμο Α (ΗS-CoA) (3)
Λαμβάνοντας υπόψη και τη συνολική
αντίδραση γλυκόλυσης (1) και την ενδιάμεση αντίδραση πυροσταφυλικού οξέος με το
συνένζυμο Α (2), η συνολική αντίδραση και των τριών σταδίων (αφού προηγουμένως
οι συντελεστές των αντιδράσεων 2 και 3, πολλαπλασιαστούν επί 2) είναι:
γλυκόζη + 10
NAD+ + 2 FAD + 4 ADP
+ 4 φωσφορικά
 6 CO2 + 10 NADH
+ 2 FADH2 +
4 ATP + 6 H+
+ θερμότητα
(4)
6 CO2 + 10 NADH
+ 2 FADH2 +
4 ATP + 6 H+
+ θερμότητα
(4)
Από την παραπάνω συνολική
αντίδραση προκύπτει ότι η ολοκληρωτική οξείδωση ενός μορίου γλυκόζης μέσω
της γλυκόλυσης, της αντίδρασης του πυροσταφυλικού με το συνένζυμο Α και του κύκλου Κrebs προσφέρει μόνο 4 μόρια ATP, αλλά
συγχρόνως παρέχει 10 μόρια NADH και 2 μόρια FADH2.
Στα 12 τελευταία μόρια έχει μετουσιωθεί η μισή αναγωγική δύναμη του μορίου
της γλυκόζης.
Η οξείδωση των ανηγμένων μορφών αυτών των συνενζύμων από το μοριακό οξυγόνο
θα δώσει πολύ περισσότερα (τυπικά 32) μόρια ATP κατά το επόμενο στάδιο της
οξειδωτικής φωσφορυλίωσης, όπως συνοπτικά περιγράφεται στη συνέχεια.
Βασική δομή των μιτοχονδρίων
[Αναφ. 8]
Τα μιτοχόνδρια είναι οργανίδια
(organelles) των κυττάρων και συχνά αποκαλούνται
"εργοστάσια παραγωγής ενέργειας". Πράγματι, το συντριπτικά
μεγαλύτερο ποσοστό της ποσότητας ATP, που χρειάζεται για να κρατάει έναν
οργανισμό ζωντανό, παράγεται
στα μιτοχόνδρια χρησιμοποιώντας την ενέργεια που βρίσκεται στην τροφή και το
οξυγόνο της αναπνοής.
Τα μιτοχόνδρια χρησιμοποιούνται από τα κύτταρα
για τον μεταβολισμό των βιολογικών μακρομορίων (υδατάνθρακες, λίπη) που
προσλαμβάνουν οι οργανισμοί με τις τροφές.
Αντίστοιχα σωματίδια στα φυτά είναι οι
χλωροπλάστες (chloroplasts), όπου ως πηγή ενέργειας χρησιμοποιούν το
ηλιακό φως.
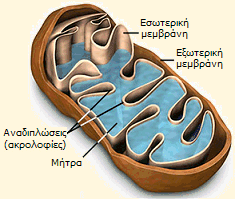
Τα μιτοχόνδρια έχουν επίμηκες,
σφαιρικό ή ωοειδές σχήμα, μήκους 0,5-2 μm. Τα βασικά δομικά χαρακτηριστικά
των μιτοχονδρίων είναι: (α) η
εξωτερική μεμβράνη με ομαλή επιφάνεια από φωσφολιποειδή, (β) η εσωτερική μεμβράνη με το πλήθος των
αναδιπλώσεών
της, οι οποίες είναι γνωστές ως ακρολοφίες (cristae). Οι ακρολοφίες αυξάνουν σημαντικά την ολική επιφάνεια της
εσωτερικής μεμβράνης σε σχέση με εκείνη της εξωτερικής
και (γ) η μήτρα (matrix) που περιβάλλεται από την εσωτερική μεμβράνη. Οι κύριες
βιοχημικές διαδικασίες (π.χ. ακετυλίωση του συνενζύμου Α και κύκλος Krebs),
όπως και η οξειδωτική φωσφορυλίωση πραγματοποιούνται στη μιτοχονδριακή μήτρα, όπου βρίσκεται μια μεγάλη ποικιλία ενζύμων.
Η εσωτερική μεμβράνη των μιτοχονδρίων
είναι αδιαπέραστη από μικρά ιόντα, αλλά είναι
διάσπαρτη από ένζυμα-ιοντικές διαύλους, που συνιστούν μια αλυσίδα
μεταφοράς ηλεκτρονίων (electron transport chain, ACT). Αντίθετα, η εξωτερική
μεμβράνη διαθέτει σχετικά μεγάλους πόρους και είναι διαπερατή από μόρια με
MB μέχρι και 10 kDa. Ουσιαστικά η εξωτερική μεμβράνη επιτρέπει την
εξισορρόπηση του υγρού του διαμεμβρανικού χώρου με το κυτταρόπλασμα που
περιβάλλει τα μιτοχόνδρια, αλλά σε συνδυασμό με τη γεωμετρία των πτυχώσεων,
αποτρέπει σε κάποιο βαθμό την άμεση διάχυση του υγρού της περιοχής αυτής στο
κυτταρόπλασμα που περιβάλλει τα μιτοχόνδρια.
Ο διαμεμβρανικός χώρος περιέχει:
(α) Μεταβολίτες οι οποίοι διαχέονται μέσω της εξωτερικής μεμβράνης. (β) ΑΤΡ που παράγεται στο μιτοχόνδριο. (γ) Ιόντα που αντλούνται από τον χώρο της
μήτρας, κατά την οξειδωτική φωσφορυλίωση.
 |
|
 |
|
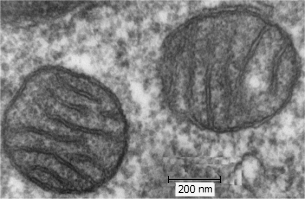
Βασικά δομικά
στοιχεία των μιτοχονδρίων [Πηγή] |
|
Μιτοχόνδρια πνευμονικού ιστού
θηλαστικών
[Πηγή] |
'Ενα τυπικό ζωικό κύτταρο
περιέχει 1000 έως 2000 μιτοχόνδρια. Το ATP παράγεται με την έμμεση καύση των
τροφών τις οποίες λαμβάνει ένας οργανισμός με το οξυγόνο που λαμβάνει μέσω της
αναπνοής. Κάθε ζωντανό κύτταρο περιέχει μιτοχόνδρια και παράγει ATP, κάτι το
οποιο δεν ισχύει στα νεκρά κύτταρα, όπως της εξωτερικής επιδερμίδας και των μαλλιών.
Κάποια κύτταρα περιέχουν περισσότερα μιτοχόνδρια, όπως τα μυϊκά κύτταρα λόγω του μηχανικού έργου που
εκτελούν. Στα θηλαστικά, τα μιτοχόνδρια καταλαμβάνουν το 15 έως 20% των
ηπατικών κυττάρων.
Οι περισσότερες βλάβες του
μεταβολισμού εντοπίζονται στα μιτοχόνδρια και στις περιορισμένες ποσότητες
διαθέσιμων ενζύμων που μετέχουν σ' αυτόν. Αύξηση των μιτοχονδρίων και των
ενζύμων που εμπεριέχονται σ' αυτά βελτιώνουν τον μεταβολισμό και στο αποτέλεσμα
αυτό μπορούν να συμβάλουν σημαντικά ήπιες σωματικές ασκήσεις αεροβικής (aerobics).
|
Οξειδωτική φωσφορυλίωση [Αναφ. 10]
Η οξειδωτική φωσφορυλίωση
(oxidative
phosphorylation) από άποψη παραγόμενης ποσότητας αποτελεί τον κύριο μηχανισμό σύνθεσης ATP
(από ADP και φωσφορικά ιόντα) στους
αερόβιους οργανισμούς και πραγματοποιείται αποκλειστικά στα μιτοχόνδρια.
Η διαδικασία της οξειδωτικής φωσφορυλίωσης μπορεί να διακριθεί σε δύο
επιμέρους μηχανισμούς: (α) τον μηχανισμό της αλυσίδας
μεταφοράς ηλεκτρονίων και (β) τον μηχανισμό της χημειώσμωσης.
|
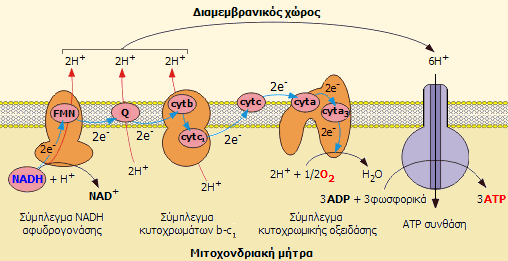
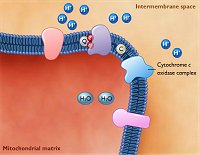
Διαδικασία
οξειδωτικής φωσφορυλίωσης: Αλυσίδα μεταφοράς ηλεκτρονίων (μπλε
βέλη)+ Χημειώσμωση. Στο σχήμα δείχνεται η διακίνηση των ηλεκτρονίων του
NADH, που ως αποτέλεσμα έχει 1 μόριό του να "αντλεί" 6 πρωτόνια
από τη μιτοχονδριακή μήτρα. Ίδια διαδρομή ακολουθεί και η διακίνηση των
ηλεκτρονίων του FADH2
με μόνη διαφορά ότι ξεκινά από το 2ο στάδιο γιαυτό και 1 μόριό
του "αντλεί" 4 πρωτόνια από τη μιτοχονδριακή μήτρα
(κόκκινα βέλη). |
Αλυσίδα
μεταφοράς ηλεκτρονίων. Η εσωτερική μεμβράνη των μιτοχονδρίων είναι
διάσπαρτη από ένζυμα-ιοντικές διαύλους, που συνιστούν μια αλυσίδα
μεταφοράς ηλεκτρονίων (electron transport chain, ETC). Αντίθετα, η εξωτερική
μεμβράνη των μιτοχονδρίων διαθέτει σχετικά μεγάλους πόρους, οι οποίοι ουσιαστικά επιτρέπουν την
εξισορρόπηση του υγρού του διαμεμβρανικού χώρου με το κυτταρόπλασμα που
περιβάλλει τα μιτοχόνδρια, αλλά αποτρέπει την άμεση διάχυση του υγρού της
περιοχής αυτής στο κυτταρόπλασμα.
Η ενέργεια που απαιτείται
για τη φωσφορυλίωση του ADP προς ATP προέρχεται από την
αναγωγή του οξυγόνου από τις ανηγμένες μορφές των οξειδοαναγωγικών συνενζύμων
NADH και FADH2 που
παρήχθησαν κατά τα προηγούμενα στάδια.
Συνεισφέρει επίσης και το NADH που παρήχθει κατά
τη γλυκόλυση και βρίσκεται στο κυτταρόπλασμα.
Ουσιαστικά, τα NADH και FADH2
φέρουν την αναγωγική δύναμη της τροφής που έχει λάβει και έχει καταβολίσει ο
οργανισμός.
Ωστόσο, η "διαδρομή" την οποία ακολουθεί η ενέργεια
και οι μορφές που αποκτά ενδιαμέσως μέχρις ότου πραγματοποιηθεί η σύνθεση του ATP, είναι κάπως περίπλοκη και ιδιαιτέρως ενδιαφέρουσα.
Τα ηλεκτρόνια τα οποία διακινούνται ως ανηγμένη μορφή των οξειδοαναγωγικών συνενζύμων (NADH,
FADH2), αφού πραγματοποιήσουν μια σειρά
"διελεύσεων" μέσω των συμπλεγμάτων ενζύμων και ενώσεων, που βρίσκονται στην εσωτερική μεμβράνη των
μιτοχονδρίων, φθάνουν στους τελικούς αποδέκτες τους που δεν είναι άλλοι παρά τα άτομα του μορίου Ο2
(από την αναπνοή) και τα ανάγουν προς ύδωρ.
Κατά τις
διελεύσεις αυτές, το ζεύγος των ηλεκτρονίων το οποίο παρέχει το κάθε μόριο NADH ή
FADH2,
αντλούνται πρωτόνια από τη μιτοχονδριακή μήτρα προς τον
διαμεμβρανικό χώρο. Κατά την άντληση αυτή, το αρχικό ενεργειακό περιεχόμενό
τους δαπανάται σταδιακά και κατά τρόπο
ελεγχόμενο και επωφελώς για τον οργανισμό (ενεργειακή "επένδυση"). Η όλη διαδικασία καταλύεται από σειρά
πολυπρωτεϊνικών συμπλεγμάτων (multiprotein compexes), αλλά και απλούστερων
ενώσεων (όπως π.χ. η λιπόφιλη κινόνη
ουβικινόνη, συνένζυμο Q ή Q10), οι οποίες βρίσκονται στην εσωτερική μεμβράνη και συνεργάζονται μεταξύ
τους για την επίτευξη των διελεύσεων αυτών. Τα εμπλεκόμενα ένζυμα
(κυτταροχρώματα) έχουν οξειδοαναγωγικό χαρακτήρα με ενεργά
κέντρα Fe(II)/Fe(III) και Cu(I)/Cu(II).
Ο τρόπος διακίνησης των
ηλεκτρονίων σε κάποιο βαθμό θυμίζει
το άθλημα της σκυταλοδρομίας, όπου το ρόλο της σκυτάλης παίζει το ζεύγος ηλεκτρονίων και
οι αθλητές είναι τα ένζυμα και οι ενώσεις που παρεμβάλλονται στη διαδρομή:
η κάθε ένωση ανάγεται από το εισερχόμενο ζεύγος ηλεκτρονίων και στη συνέχεια οξειδώνεται
μεταβιβάζοντας το ζεύγος ηλεκτρονίων στην επόμενη κ.ο.κ.
Το καθαρό αποτέλεσμα αυτών των διελεύσεων είναι: 1 ζεύγος ηλεκτρονίων
προερχόμενο από ένα μόριο NADH ανάγει όχι άμεσα αλλά κατά στάδια 1 άτομο οξυγόνου,
σύμφωνα με την παρακάτω συνολική αντίδραση, προκαλώντας τη μεταφορά
συνολικώς 6 πρωτονίων από τη μιτοχονδριακή μήτρα στον διαμεμβρανικό χώρο:
NADH
+ H+ + 1/2
O2
 NAD+ + H2O Η
αντίδραση αυτή προκαλεί και τη μεταφορά: 6 Η+
(από τη μήτρα)
NAD+ + H2O Η
αντίδραση αυτή προκαλεί και τη μεταφορά: 6 Η+
(από τη μήτρα)
 6 Η+ (στον διαμεμβρανικό χώρο)
6 Η+ (στον διαμεμβρανικό χώρο)
Ανάλογη είναι και τύχη του FADH2:
FADH2
+ 1/2 O2
 FAD + H2O
Η αντίδραση αυτή προκαλεί και τη μεταφορά: 4 Η+
(από τη μήτρα)
FAD + H2O
Η αντίδραση αυτή προκαλεί και τη μεταφορά: 4 Η+
(από τη μήτρα)
 4 Η+ (στον διαμεμβρανικό χώρο)
4 Η+ (στον διαμεμβρανικό χώρο)
Η αρχική χημική ενέργεια των NADH
και FADH2 τώρα έχει αλλάξει
μορφή. 'Εχει πλέον μετατραπεί σε
δυναμική ενέργεια λόγω της διαφοράς των συγκεντρώσεων (βαθμίδας
συγκέντρωσης) των πρωτονίων από τις δύο πλευρές της εσωτερικής μεμβράνης, δηλ. μεταξύ
του διαμεμβρανικού χώρου (με πλεόνασμα πρωτονίων) και της μιτοχονδριακής μήτρας
(με έλλειμμα πρωτονίων). Επομένως, ο χώρος της μήτρας είναι
αρνητικά φορτισμένος ως προς τον διαμεμβρανικό χώρο. Η στενότητα του
τελευταίου σε συνδυασμό με τις αναδιπλώσεις της εσωτερικής μεμβράνης δεν
επιτρέπουν ουσιαστικά τη διάχυση των πρωτονίων εκτός μιτοχονδρίων.
Η κατάσταση είναι
ανάλογη με την αποθήκευση ηλεκτρικής ενέργειας σε έναν φορτισμένο
πυκνωτή, υπό τη μορφή διαχωρισμένου ηλεκτρικού φορτίου (θετικού/αρνητικού)
και όπου η ενέργεια αυτή μπορεί να αποδοθεί π.χ. ως θερμική, κατά την εκφόρτιση
του πυκνωτή (επανασύνδεση ηλεκτρικού φορτίου) μέσω μιας ωμικής αντίστασης. Στην προκειμένη περίπτωση
αυτή η "εκφόρτιση" πραγματοποιείται με τη χημειώσμωση και το εκπληκτικό ένζυμο ATP-συνθάση, η δε ενέργεια
δεν θα διαχυθεί ως θερμότητα, αλλά θα αποθηκευτεί ως χημική ενέργεια σε νέα μόρια ATP.
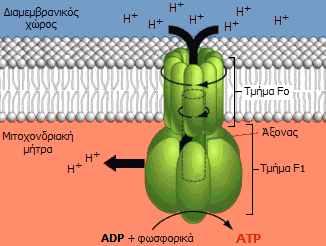
ATP-συνθάση και χημειώσμωση. Στο τελικό στάδιο (φωσφορυλίωση του ADP προς ATP)
πραγματοποιείται από ένα ογκώδες ένζυμο (600 kDa) - "μοριακή μηχανή", την
ATP-συνθάση (ATP
synthase). Ο τρόπος λειτουργίας αυτού
του ενζύμου είναι ΕΚΠΛΗΚΤΙΚΟΣ
στις λεπτομέρειές του.
Η αξιοποίηση των διαφορών
συγκεντρώσεων Η+ (βαθμίδα [Η+]) για την παραγωγή έργου
σε ένα κύτταρο αναφέρεται ως χημειώσμωση (chemiosmosis) και η σχετική
θεωρία διατυπώθηκε για πρώτη φορά από τον Βρετανό βιοχημικό
Peter Mitchell (1920-1992) κατά τη δεκαετία του 1960. Η θεωρία του ήταν
πολύ δύσκολο να γίνει αποδεκτή με τις μέχρι τότε αντιλήψεις, ωστόσο, για τη θεωρία
του αυτή ο Mitchell τιμήθηκε με το βραβείο
Nobel Χημείας του 1978.
Η οξειδωτική φωσφορυλίωση οι
μεταμορφώσεις της ενέργειας ακολουθούν το παρακάτω μάλλον παράδοξο σχήμα:

Η μεγαλύτερη συγκέντρωση
των πρωτονίων στον διαμεμβρανικό χώρο σε σχέση με τη συγκέντρωσή τους στη μιτοχονδριακή μήτρα,
προκαλεί μια αυθόρμητη συνεχή ροή
των πρωτονίων από τον πρώτο χώρο στον δεύτερο, μέσω ενός διαύλου που παρέχει η ATP-συνθάση.
Η ελεύθερη ενέργεια που απελευθερώνεται με αυτήν την αυθόρμητη ροή αξιοποιείται
για τη σύνθεση του ATP. Η ροή των πρωτονίων έχει αποτέλεσμα την περιστροφή ενός τμήματος του ενζύμου,
όπως
το νερό προκαλεί τη ροή ενός νερόμυλου! Και η ροή αυτή είναι συνεχής, αφού
συνεχώς λειτουργεί και η αλυσίδα μεταφοράς ηλεκτρονίων που περιγράφηκε
προηγουμένως.
Διακρίνονται δύο χαρακτηριστικά
τμήματα στην ATP-συνθάση: Το λιπόφιλο τμήμα Fo
που περιβάλλεται από την εσωτερική
μεμβράνη και το υδρόφιλο τμήμα F1
το οποίο προεξέχει και βρίσκεται στη μιτοχονδριακή μήτρα. Αποτελείται από 6
υπομονάδες: Τρεις όμοιες υπομονάδες με καταλυτικές θέσεις, εναλλάξ με τρεις
όμοιες υπομονάδες χωρίς.
Καθώς διέρχονται τα πρωτόνια μέσω
ενός πλευρικού στατικού διαύλου προκαλούν κουλομβικές απώσεις σε θετικώς
φορτισμένα σημεία των υπομονάδων που συνθέτουν το τμήμα Fo
αυτό προκαλώντας την
περιστροφή του σε βήματα των 120º.
Απαιτείται μια επαναρροή 8 έως 15 πρωτονίων στη μιτοχονδριακή μήτρα για μια πλήρη περιστροφή του
τμήματος Fo,
ανάλογα με το ζωικό είδος. Ο "ρότορας" του ενζύμου περιστρέφεται περίπου 100 φορές το δευτερόλεπτο.
'Ενα σύμπλεγμα ATP-συνθάσης παράγει 100-150 μόρια ATP το δευτερόλεπτο.
Με βάση αυτούς τους ρυθμούς εκτιμάται πως κατά μέσο όρο ο άνθρωπος
δημιουργεί ημερησίως ποσότητα ATP ίση με το βάρος του.
|
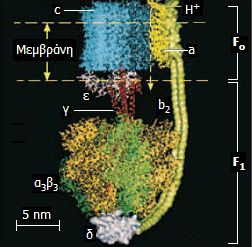
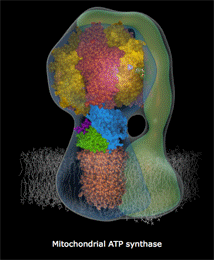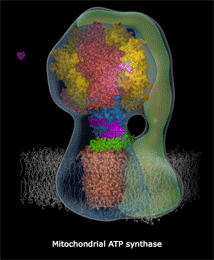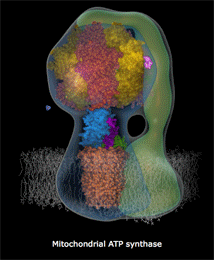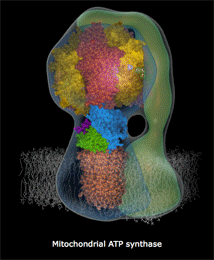
Αριστερά: Σχηματικό μοντέλο της ATP-συνθάσης και θέση της
στην εσωτερική μεμβράνη των μιτοχονδρίων. Κέντρο: Μοριακό
μοντέλο όπου δείχνονται οι επιμέρους υπομονάδες που συγκροτούν
την ATP-συνθάση: στατικό τμήμα F1 (α3β3γεδ),
περιστρεφόμενο Fo (ab2c10-14)
[Αναφ. 10θ].
Δεξιά:
Κινούμενο σχέδιο που δείχνει τις
φάσεις σύνθεσης του ATP. Τα σωματίδια ATP δείχνεται κόκκινα, του ADP και
των φωσφορικών ροζ. Το περιστρεφόμενο τμήμα (Fo) του ενζύμου
συνδέεται με τον έκκεντρο άξονα (μαύρος) (πηγή: [Αναφ. 8β]). |
Την περιστροφή του τμήματος Fo
(ρότορας του "μοριακού κινητήρα") παρακολουθεί
μια ασύμμετρη υπομονάδα του ενζύμου που αναφέρεται στο παραπάνω σχήμα ως άξονας,
η οποία καθώς περιστρέφεται
προκαλεί διαδοχικές παραμορφώσεις και πιέσεις στις καταλυτικές υπομονάδες που συνιστούν το τμήμα
F1.
Το τμήμα αυτό δρα σαν μηχανή "συναρμολόγησης":
Παραλαμβάνει ένα μόριο ADP και ένα φωσφορικό ιόν
και τα "συναρμολογεί" σχηματίζοντας ένα μόριο
ATP!
Σε τρεις φάσεις
πραγματοποιούνται: (α) Η "σύλληψη" του ADP και του
φωσφορικού ιόντος, (β) η σύνδεσή τους με σχηματισμό ATP
και (γ) η απελευθέρωση του σχηματισμένου ATP
προς τη μιτοχονδριακή μήτρα, από την οποία διαχέεται προς τον διαμεμβρανικό
χώρο και τελικά προς το κυτταρόπλασμα. Ουσιαστικά, το ένζυμο μετασχηματίζει
την κινητική ενέργεια σε χημική ενέργεια. Σε κάθε
μία πλήρη περιστροφή πραγματοποιείται η σύνθεση μέχρι και τριών μορίων
ATP, όπως δείχνονται παραστατικά στο παραπάνω κινούμενο
σχέδιο.
Κάτι ακόμη
εκπληκτικό: 'Εχει αποδειχθεί
πειραματικά η αντιστρεπτότητα της δράσης του
ενζύμου: Περιστροφή του "ρότορα" κατά την αντίστροφη φορά
επιφέρει διάσπαση του ATP και μεταφορά πρωτονίων κατά την
αντίθετη κατεύθυνση.
Ο μηχανισμός λειτουργίας του
ενζύμου διευκρινίστηκε από τους
Paul D. Boyer (University of California) και
John E. Walker, (Cambridge, Μ. Βρετανίας), οι οποίοι
τιμήθηκαν για την ανακάλυψή τους με το βραβείο Nobel Χημείας του 1997.
Λεπτομερέστερες περιγραφές της δομής και της λειτουργίας της ATP-συνθάσης
μπορούν να αναζητηθούν στη βιβλιογραφία [Αναφ.
10στ-θ].
 |
 |
 |
|
 |
 |
|
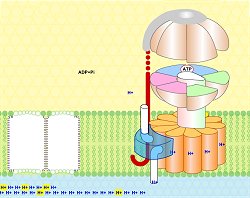
Κινούμενο σχέδιο που
δείχνει πως περίπου περιστρέφεται το τμήμα Fo
της ATP-συνθάσης και παράγεται το ATP [Πηγή]. |
Κινούμενο
σχέδιο που δείχνει τα στάδια σύνθεσης ATP
με τη μηχανή της ATP-συνθάσης
[Πηγή]. |
|
Paul D. Boyer (University of California) |
John E. Walker, (Cambridge, Μ. Βρετανίας) |
Συνθάση ή συνθετάση;
Υπάρχει διαφορά μεταξύ των
ονομασιών συνθάση (synthase) και
συνθετάση (synthetase). Ως συνθάσες
χαρακτηρίζονται τα ένζυμα που καταλύουν μια βιοχημική αντίδραση σύνθεσης
χωρίς να αντλούν ενέργεια από ATP, σε αντίθεση με
τις συνθετάσες που καταλύουν αντιδράσεις σύνθεσης αντλώντας ενέργεια
από ATP. Επειδή συχνά οι ονομασίες συνθάση και
συνθετάση συγχέονται, η ενιαία επιτροπή βιοχημικής ορολογίας συνιστά τον όρο
λιγάση (ligase, από το λατινικό ρήμα
ligare: συνδέω, συγκολλώ)
αντί του όρου συνθετάση (JCBN/NC-IUB
Newsletter 1984) [Πηγή]. |
Ενεργειακό ισοζύγιο
Για κάθε 2 επανερχόμενα πρωτόνια
μέσω της ATP-συνθάσης αποδίδεται ενέργεια που
προκαλεί φωσφορυλίωση 1 μορίου ADP προς
ATP. Με βάση τα προηγούμενα 1 μόριο
NADH "αξίζει" 3 μόρια ATP
και ένα μόριο FADH2 "αξίζει" 2 μόρια
ATP, οπότε από τη συνολική αντίδραση 4 ανά μόριο
γλυκόζης θα παραχθούν:
(μόρια
ATP)ολικά
= (μόρια
NADH) x
3
+ (μόρια
FADH2)
x 2
+
(μόρια
ATP) = 10
x 3
+ 2 x 2 + 4 = 38
Εδώ συνυπολογίζονται τα 2
μόρια NADH που παράγονται κατά τη γλυκόλυση.
Ωστόσο, αυτά παράγονται στο κυτταρόπλασμα
και όχι στη μιτοχονδριακή μήτρα όπως τα υπόλοιπα 8. Η μεταφορά τους στη
μήτρα πραγματοποιείται κατά έμμεσο τρόπο, αφού η εσωτερική μεμβράνη δεν
είναι διαπερατή από τα
μόρια NADH. Στην ουσία δεν μεταφέρονται τα ίδια, αλλά η αναγωγική ισχύς τους μέσω συζευγμένων
αντιδράσεων και με κατανάλωση ενέργειας ισοδύναμης με 1 μόριο
ATP ανά μόριο NADH,
οπότε το καθαρό αποτέλεσμα είναι:
1 μόριο γλυκόζης ενεργειακά ισοδυναμεί με
36 μόρια ATP
Στην πραγματικότητα, πάντοτε
υπάρχουν ενεργειακές απώλειες, οπότε ο αριθμός 36 θα πρέπει να θεωρηθεί ως ο μέγιστος
εφικτός.
Ενεργειακή απόδοση: Η ενεργειακή
απόδοση της όλης διαδικασίας είναι: (36
mol ATP/mol γλυκόζης) x
(7,3 kcal/mol ATP) x 100
/ (686 kcal/mol γλυκόζης)
= 42 %
|
-
Με τις παραπάνω διεργασίες παραλαμβάνεται περίπου το 40% της
ενέργειας που παρέχει η γλυκόζη
- 'Ενα συμβατικού τύπου
αυτοκίνητο αξιοποιεί μόνο το 25% της ενέργειας που παρέχουν τα
καύσιμά του |
Λιπαρά
οξέα. Ανάλογες διαδρομές ακολουθούν και οι καταβολισμοί των
λιπών. Οι εστέρες της γλυκερίνης υδρολύονται και η γλυκερίνη εισέρχεται στη
διαδρομή της γλυκόλυσης ως φωσφογλυκεραλδεΰδη και από εκεί και πέρα
ακολουθεί τη διαδρομή που περιγράφηκε προηγουμένως. Τα λιπαρά οξέα
οξειδώνονται με μια διεργασία γνωστή ως
β-οξείδωση (beta oxidation). Κατά τη διεργασία αυτή τα μόρια των
λιπαρών οξέων διασπώνται σταδιακά (σε τμήματα δύο ανθράκων) για να σχηματίσουν ακετυλο-συνένζυμο Α, το οποίο υπεισέρχεται στο κύκλο Krebs. Tα συνολικώς
παραγόμενα NAD και FADH2
υπεισέρχονται στην αλυσίδα μεταφοράς ηλεκτρονίων, όπως συνοπτικά περιγράφηκε
προηγουμένως.
Για ένα κορεσμένο οξύ με 2n
άνθρακες μπορεί με ανάλογους όπως προηγουμένως υπολογισμούς να δειχθεί ότι
ισχύει η σχέση:
(μόρια
ATP)ολικά
= (n - 1) x 14 +
8
Έτσι, π.χ. ο καταβολισμός ενός μορίου παλμιτικού οξέος, CΗ3[CH2]14COOH,
(με 2n = 16) παρέχει συνολικά: (μόρια
ATP)ολικά
= (8 - 1) x 14 + 8 = 106
Αναλυτικός προσδιορισμός ATP
[Αναφ. 11]
|

Η λουσιφεράση είναι
ένα ένα ένζυμο που λαμβάνεται από τις πυγολαμπίδες |
Η καθιερωμένη μέθοδος προσδιορισμού ATP σε
βιολογικά υγρά είναι εξαιρετικά απλή και βασίζεται στη
βιοφωταύγεια (bioluminescence).
Το ATP αντιδρά με
λουσιφερίνη
(luciferin) παρέχοντας μια ενδιάμεση ένωση, την αδενυλολουσιφερίνη, παρουσία του
ενζύμου λουσιφεράση
(luciferase), το ένζυμο που καταλύει την εκπομπή βιοφωταύγειας από τις
πυγολαμπίδες, και παρουσία μικρής συγκέντρωσης ιόντων μαγνησίου, σε pH 7,8. Η ενδιάμεση ένωση
αντιδρά με το διαλυμένο οξυγόνο παρέχοντας βιοφωταύγεια (με λmax = 560 nm), της
οποίας η ένταση συσχετίζεται γραμμικά με την ποσότητα ATP του εξεταζόμενου
δείγματος.
Ο βιοφωταυγειομετρικός προσδιορισμός του
ATP είναι εξαιρετικά απλός, με μεγάλη
εκλεκτικότητα και ιδιαίτερα ευαίσθητος με κατώτερο όριο ανίχνευσης ποσότητες ATP
της τάξης του 0,1 pmol ATP (50 pg). Ο προσδιορισμός είναι ιδιαίτερα χρήσιμος
στην έρευνα για την ανίχνευση της παραγωγής ATP σε διάφορες ενζυματικές
αντιδράσεις, για τον προσδιορισμό της ενεργότητας των σχετικών ενζύμων.
Το ATP χάνεται γρήγορα
στα νεκρά κύτταρα, αφού δεν λειτουργεί πλέον σ' αυτά η αναπνευστική αλυσίδα για
την αναπλήρωσή του. Οπότε,
μια ιδιαίτερα χρήσιμη εφαρμογή του βιοφωταυγειομετρικού προσδιορισμού του ATP είναι η
ανίχνευση ζώντων κυττάρων, μικροοργανισμών και βακτηριακής μόλυνσης σε δείγματα
τροφίμων, αίματος, ούρων,
γάλατος, χώματος και αποβλήτων. Η μέθοδος αυτή παρέχει άμεσα αποτελέσματα σε
αντίθεση με τη συμβατική μέθοδο των μικροβιακών καλλιεργειών, όπου συχνά απαιτούνται
αρκετές ημέρες μέχρι να αναπτυχθούν ορατές αποικίες μικροβίων.
Για τον σκοπό αυτό διατίθενται στο εμπόριο εύχρηστα φορητά φωταυγειόμετρα (βλ.
σχήμα παρακάτω).
Η ίδια μέθοδος χρησιμοποιείται και στην έρευνα για την αντιμετώπιση του
καρκίνου. Με τον βιοφωταυγειομετρικό προσδιορισμό του ATP είναι δυνατόν να διακριθεί αν η δράση ενός
νέου αντικαρκινικού φαρμάκου σε ένα καρκινικό κύτταρο είναι κυτταροστατική ή
κυτταροτοξική.
 |
 |
|
|
Φωταυγειόμετρα (luminometers)
εργαστηριακού πάγκου [πηγή]
και φορητό [πηγή].
Το τελευταίο χρησιμοποιείται κυρίως για την ταχεία ανίχνευση
μικροοργανισμών σε τρόφιμα. |
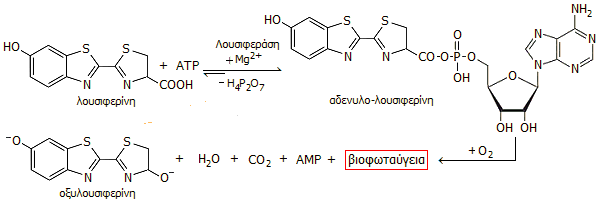
Αλληλουχία αντιδράσεων
κατά το βιοφωταυγειομετρικό προσδιορισμό ATP.
|
 |
 |
 |
 |
 |
|
Μερικά ακόμη από τα άφθονα εκπαιδευτικά video
που υπάρχουν στο YouTube και στο διαδίκτυο γενικότερα πάνω στη δράση του ATP και στη σύνθεσή του
στα μιτοχόνδρια. |
Βιβλιογραφία -
Πηγές από το Διαδίκτυο
1. (α) Merck Index, 12th ed, σελ.
28 (adenosine triphosphate). (β) Wikipedia:
"Adenosine
triphosphate".
(γ)
Delepine A-S, Tripier R, Handel H: "Cyclen-based bismacrocycles for
biological anion recognition. A potentiometric and NMR study of AMP, ADP and ATP
nucleotide complexation", Org. Biomol. Chem. 6:1743-1750, 2008 (Abstract).
2. (α) Langen P, Hucho F: "Karl
Lohmann and the Discovery of ATP", Angew Chem Int Ed Engl. 47(10):1824-1827,
2008 (το κείμενο μπορεί να
βρεθεί εδώ).
(β) Wikipedia: "Karl
Lohmann (Biochemiker)". (γ)
www.nndb.com: "Karl
Lohmann".
(γ)
Simoni RD, Hill RL, Vaughan M: "The
Determination of Phosphorus and the Discovery of Phosphocreatine and ATP: the
Work of Fiske and SubbaRow",
J. Biol. Chem. 277:e21,
2002. (δ)
Lohmann K:
"Über
die Pyrophosphatfraktion im Muskel",
Naturwissenschaften 17(31):624-625,
1929 (Abstract,
1η
σελ.).
(ε) Fiske CH, SubbaRow Y: "Phosphorous
compounds of muscle and liver", Science
70(1816):381-382, 1929 (Abstract).
(στ) Fiske CH,
SubbaRow Υ:
"Phosphocreatine",
J. Biol. Chem. 81:629-679, 1929.
(ζ)
Fiske CH,
SubbaRow Υ:
"The Colorimetric Determination of Phosphorus", J. Biol. Chem. 66:375-400,
1925.
(η) Fiske CH: "The
Nature of the Depressor Substance of the Blood", Proc Natl Acad Sci USA
20(1): 25-27, 1934. (θ)
Baddiley J,
Michelson AM, Todd AR:
"Synthesis of Adenosine Triphosphate",
Nature 161,
761-762, 1948 (Abstract).
(ι)
"Nature's
Batteries' May Have Helped Power Early Lifeforms", Science Daily, May 25,
2010. (ια)
Δημόπουλος ΚΑ, Αντωνοπούλου Σ: "Βασική
Βιοχημεία" (Κεφ. "Εισαγωγή στο μεταβολισμό", σελ. 321-334), 2η έκδοση,
2009.
3. (α)
Greenwood NN, Earnshaw A: "Chemistry of the
Elements", Pergamon Press, 1st ed. 1984, σελ. 608-611. (β) Wikipedia: "Polyphosphate".
(γ) SPER Chemical Corporation: "Polyphosphate:
Effective Sequestering Agent for Potable Water Systems",
2010.
4. (α)
Thermo Scientific Co: "ATP".
(β) Sigma Co., Product information: "Adenosine 5'-triphosphate
di(tris) salt dihydrate" (αρχείο
PDF, 50 KB). (γ)
Rayment I, Allingham J: "Myosin
Motors: The Chemical Restraints Imposed by ATP", Controlled Nanoscale Motion
Lecture Notes in Physics, 711:15-40, 2007 (αρχείο
PDF, 2,8 MB).
5.
(α) phosphorus.atomistry.com: "Phosphorus
Pentoxide, P2O5".
(β)
Gajewski E, Steckler DK, Goldberg RN: "Thermodynamics
of the Hydrolysis of Adenosine 5''triphosphate to Adenosine 5'-diphosphate", J. Biol. Chem.
261(27):12733-12737, 1986 (αρχείο
PDF, 516 KB). (γ) Wilson JE, Chin A: "Chelation of divalent cations by ATP,
studied by titration calorimetry", Analytical Biochemistry 193(1):16-19, 1991
(Abstract).
6. Todd A: "Synthesis in the
study of nucleotides", Nobel Lecture, December 11, 1957 (αρχείο
PDF, 99 KB).
7.
Maxwell R:
"Daily
Newsletter: October 2, 2012 - Glycolysis part 2",
Biology MOOC Newsletter Archive,
Georgia State University."
8. (α) Wikipedia: "Mitochondrion".
(β) Georgia State University: "Mitochnondria".
(γ) Willett K: "Mitochondria:
The aerobic engines", BikeTech Review, May 2006.
9. (α) University of Illinois: "Glycolysis,
Krebs Cycle, and other Energy-Releasing Pathways". (β) Wikipedia: "Oxidative
Phosphorylation".
10. (α)
Rensselaer Polytechnic
Institute: "Oxidative
Phosphorylation: Chemiosmotic Coupling". (β) University of Cambridge, Medical
Research Council: "Mitochondrial
Biology Unit: ATP Synthase". (γ) Allchin D: "Peter
Mitchell & How Cells make ATP" (αρχείο PDF, 16,2 MB). (δ) San Diego
State University: "Ch.
XXII. Oxidative Phosphorylation". (ε)
Casiday R, Herman C, Frey R:
"Energy
for the Body: Oxidative Phosphorylation - Oxidation-Reduction Reactions
Experiment", Department of Chemistry, Washington University St. Louis.
(στ) Nicholson D: "ATP
synthase",
Sigma-Aldrich.
(ζ) Boyer P: "A
Research Journey with ATP Synthase",
Journal of Biological Chemistry 277(42):39045-39061, 2002. (η)
Dickson VK, Silvester JA,
Fearnley IM, Leslie AGW, Walker JE: "On
the structure of the stator of the mitochondrial ATP synthase",
The EMBO Journal 25:2911-2918,
2006.
(θ)
Xing J, Liao
J-C, Oster G: "Making
ATP",
Proc.
Natl. Acad. Sci. 102:16539-16546,
2005. (ι) Crofts A: "Lecture
10: ATP Synthase",
Biophysics 354, University of Illinois at Urbana-Champaign. (ια)
Watt IN, Montgomery MG, Runswicka MJ, Leslie AGW,
Walker JE: "Bioenergetic
cost of making an adenosine triphosphate molecule in animal mitochondria",
PNAS, 16823-16827, 2010.
11. (α) Sigma-Aldrich: "Adenosine
5′-triphosphate (ATP) Bioluminescent Assay Kit". (β) bmglabtech.com: "The
use of an ATP bioluminescence assay to quantify cell cytotoxicity". (γ)
LuminUltra Technologies Ltd.: "Τhe Science of 2nd
Generation ATP Monitoring", Document v1.5, 2011 (αρχείο
PDF, 267 KB). (δ) Long
A: "Chemiluminescence,
Bioluminescence,
and the Luciferin-Luciferase ATP Detection Assay",
University of Connecticut, 2011 (Power
Point presentation, 8,86 MB). (ε)
Chollet R, Ribault S: "Use
of ATP Bioluminescence for Rapid Detection and
Enumeration of Contaminants: The Milliflex Rapid Microbiology Detection
and Enumeration System", Bioluminescence - Recent
Advances in Oceanic Measurements and Laboratory Applications, Dr. David Lapot,
2012 (αρχείο
PDF, 1,33 MB).
(στ) Rhedin AS,
Tidefelt U, Jönsson K, Lundin A, Paul C:
"Comparison of a
bioluminescence assay with differential staining cytotoxicity for cytostatic
drug testing in vitro in human leukemic cells",
Leuk Res. 17(3):271-276,
1993 (PubMed).
|
Αποποίηση
ευθυνών:
Έχει καταβληθεί κάθε προσπάθεια για να εξασφαλισθεί η ορθότητα των
πληροφοριών που περιλαμβάνονται σε αυτή τη σελίδα, ωστόσο ο έχων την
επιμέλεια της σελίδας αυτής και το Τμήμα Χημείας δεν αναλαμβάνουν τη
νομική ευθύνη για τυχόν σφάλματα, παραλείψεις ή ανακριβείς πληροφορίες.
Επιπλέον, το Τμήμα Χημείας δεν εγγυάται την ορθότητα των αναφερόμενων σε
εξωτερικές ιστοσελίδες, ούτε η αναφορά μέσω συνδέσμων (links) στις ιστοσελίδες αυτές, υποδηλώνει ότι το Τμήμα
Χημείας επικυρώνει ή καθ' οιονδήποτε τρόπο αποδέχεται το περιεχόμενό
τους. |